
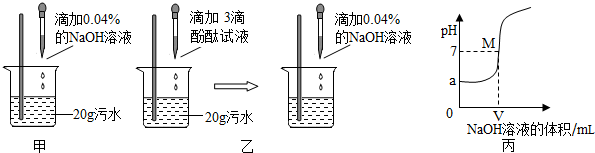
分析 (1)根据pH值的正确测定方法来考虑,否则测得的结果会产生误差进行分析;
(2)根据紫色石蕊试液在碱性溶液为蓝色进行分析;
(3)根据无色酚酞在酸性、碱性、中性溶液中的颜色分析反应的程度并通过化学方程式进行计算;
(4)根据图象中的坐标分析;
(5)根据酸的性质及可操作性、经济性等分析.
解答 解:(1)测PH值的正确测定方法是:取pH试纸放在玻璃片上,用玻璃棒蘸取待测溶液沾在pH试纸上,将试纸显示的颜色与标准比色卡比较,即可得到PH值,所以乙同学、丙同学操作都是错误的,用蒸馏水将pH试纸润湿再测该酸性溶液PH值,结果会偏大,所以操作规范的是甲同学;
(2)紫色石蕊在碱性环境中显蓝色,滴加3滴紫色石蕊试液,溶液呈深蓝色,说明此时的溶液显碱性,氢氧化钠溶液过量;
(3)盐酸和氢氧化钠反应生成氯化钠和水,酚酞试液在酸性废水中无色,当滴加氢氧化钠的过程中,当溶液刚好由无色变为红色时恰好完全反应;
设污水中H2SO4的质量分数为x,
HCl+NaOH═NaCl+H2O
36.5 40
20gx 2g×0.04%
$\frac{36.5}{20gx}$=
x=0.00365%
所以污水中HCl的质量分数为0.00365%;
(4)从曲线上可知污水的pH=a,即曲线的起点;M点的pH=7,溶液呈现中性,说明酸碱恰好完全反应;稀盐酸和氢氧化钠反应生成氯化钠和水;
(5)NaOH;Ca(OH)2;CuO;Fe四种物质都能够和盐酸发生反应,但从经济的角度考虑,氢氧化钙最便宜,故选:B.
故答案为:(1)甲;
(2)不正确,氢氧化钠溶液过量,使紫色石蕊显蓝色;
(3)防止氢氧化钠过量,使反应充分进行,溶液刚好由无色变为红色,0.00365;
(4)a,恰好完全反应;
(5)B.
点评 本题考查了酸碱度的测定方法的评价,酸碱性与pH的关系以及酸碱中和反应的运用等,综合性较强,但难度不大,关键还是熟练掌握溶液酸碱性、酸碱度测定的方法及酸碱中和反应的原理.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
| A. | 酒精做燃料 C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O 氧化反应 | |
| B. | 电解水制取氢气 2H2O$\frac{\underline{\;电解\;}}{\;}$2H2+O2 分解反应 | |
| C. | 制取少量硫酸铜溶液 H2SO4+CuCl2═CuSO4+2HCl 复分解反应 | |
| D. | 碳还原氧化铜 2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ 置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 酸、碱和盐是初中阶段化学学习的重要内容,根据它们相互间的反应现象进行合理推断更是同学们必须具备的综合能力,飞飞同学的具体实验操作流程示意图如下:
酸、碱和盐是初中阶段化学学习的重要内容,根据它们相互间的反应现象进行合理推断更是同学们必须具备的综合能力,飞飞同学的具体实验操作流程示意图如下:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 物质 | 所需时间 | 价格 |
| Fe | 约14000秒 | 10元/1000克 |
| Zn | 约50秒 | 10元/500克 |
| Mg | 约20秒 | 10元/25克 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 图为“XX”钙片商品标签图,请根据标签的有关信息完成下列各题:
图为“XX”钙片商品标签图,请根据标签的有关信息完成下列各题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 某化合物在纯氧中燃烧只生成二氧化碳和水,所以该化合物一定含碳、氢元素 | |
| B. | 燃烧一般都伴随发光和放热现象,所以有发光和放热现象的变化一定是燃烧 | |
| C. | 碱溶液的pH>7,所以pH>7的溶液一定是碱溶液 | |
| D. | 溶液中析出晶体,溶质的质量减小,所以溶质的质量分数一定减小 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 溶质质量 | B. | 溶剂质量 | C. | 溶液质量 | D. | 溶质质量分数 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
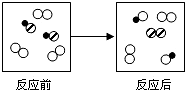 如图所示的微观变化与下列反应及反应类型对应正确的是( )
如图所示的微观变化与下列反应及反应类型对应正确的是( )| A. | 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2化合反应 | B. | 2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+I2分解反应 | ||
| C. | 2HI+Cl2═2HCl+I2置换反应 | D. | 2HCl+CuO═CuCl2+H2O复分解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com