
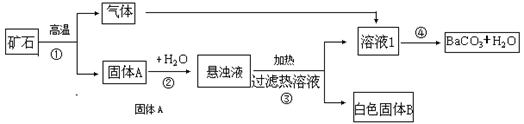
| 温度(℃) | 0 | 20 | 25 | 60 |
| Ba(OH)2溶解度 | 1.67 | 3.89 | 5.60 | 20.94 |
| Ca(OH)2溶解度 | 0.189 | 0.173 | 0.148 | 0.121 |


科目:初中化学 来源:不详 题型:推断题
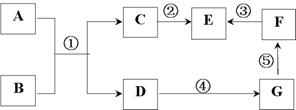
查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题
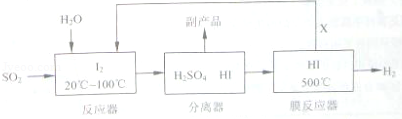
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.NaCl、Na2CO3、Ca(NO3)2、HCl | B.Na2SO4、BaCl2、K2CO3、KNO3 |
| C.FeCl3、NaOH、H2SO4、Ba(OH)2 | D.K2CO3、H2SO4、KNO3、BaCl2 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题
 ="=" NH3↑+HCl↑
="=" NH3↑+HCl↑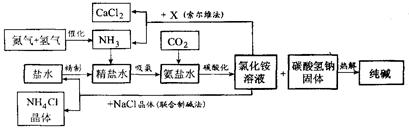
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| | 物 质 | 杂 质 | 除杂试剂 | 提 纯 方 法 |
| A | CO2 | CO | O2 | 点燃 |
| B | KCl | MnO2 | 水 | 充分溶解、过滤、蒸发 |
| C | NaCl | Na2CO3 | 硝酸 | 足量加入硝酸溶液 |
| D | Cu(NO3)2溶液 | AgNO3 | Cu粉 | 加入少量的铜粉,过滤 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| 选项 | 待鉴别的物质 | 鉴别方法 |
| A | 空气和氧气 | 用带火星的木条,观察是否复燃 |
| B | 棉纤维和羊毛纤维 | 点燃,闻燃烧产生的气味 |
| C | 海水和蒸馏水 | 加硝酸银溶液,观察是否变浑浊 |
| D | 碳酸钠溶液、石灰水 | 分别滴加无色酚酞,观察溶液是否变红 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.用水鉴别硝酸铵固体和氢氧化钠固体 |
| B.用紫色石蕊溶液鉴别二氧化碳气体和一氧化碳气体 |
| C.用稀盐酸除去氯化钠溶液中混有的少量碳酸钠 |
| D.用稀盐酸除去铁粉中混有的少量镁粉 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com