
 Fe+2HCl;该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应.
Fe+2HCl;该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应. Fe3O4;该反应符合“多变一”的特征,属于化合反应.
Fe3O4;该反应符合“多变一”的特征,属于化合反应. Fe+2HCl;置换;(2)3Fe+2O2
Fe+2HCl;置换;(2)3Fe+2O2 Fe3O4;化合.
Fe3O4;化合.

科目:初中化学 来源: 题型:阅读理解
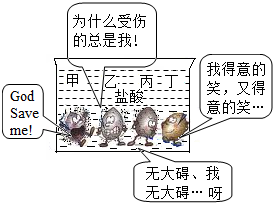
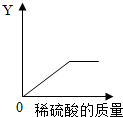
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:

| 固体 | 溶液(写出溶质的化学式) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com