
| A. | 只含有Mg2+、SO42- | |
| B. | 一定含有K+、Mg2+、Cl-、SO42- | |
| C. | 一定含有Mg2+、SO42-,可能含有Cl-、K+ | |
| D. | 一定含有Cl-、K+,可能含有Mg2+、SO42- |
分析 根据已有的知识进行分析,钡离子与硫酸根离子结合生成的硫酸钡是不溶于酸的白色沉淀,氢氧根离子能与镁离子结合生成氢氧化镁白色沉淀,氢氧化镁是溶于酸的沉淀,据此解答即可.
解答 解:①取一份废液,加入氯化钡溶液有白色沉淀产生,钡离子能与硫酸根离子结合产生硫酸钡白色沉淀,钡离子能与碳酸根离子结合产生碳酸钡白色沉淀,再加入足量稀盐酸,沉淀无变化,说明生成的是硫酸钡沉淀,不是碳酸钡沉淀,故废液中一定含有硫酸根离子,一定不含有碳酸根离子,由于有硫酸根离子,故一定不会含有钡离子;
②另取一份废液,加入氢氧化钾溶液出现白色沉淀,镁离子能与氢氧根离子结合生成溶于盐酸的氢氧化镁沉淀,故废液中一定含有镁离子;
通过分析可以知道,废液中可能含有氯离子和钾离子;
A、溶液中还可能含有Cl-和K+,故A错误;
B、溶液中不一定含有Cl-和K+,故B错误;
C、溶液中一定含有Mg2+、SO42-,可能含有Cl-、K+,故C正确;
D、溶液中不一定含有Cl-、K+,一定含有Mg2+、SO42-,故D错误;
故选C.
点评 本题考查了常见离子的检验,完成此题,可以依据已有的关于离子的性质进行.要求同学们加强对离子性质的掌握,以便灵活应用.


科目:初中化学 来源: 题型:选择题
| A. | CO和CO2都具有还原性 | |
| B. | CO和CO2均能与H2O反应 | |
| C. | CO和CO2都能用于灭火 | |
| D. | CO和CO2在一定条件下可以相互转化 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  量取20.2mL水 | B. | 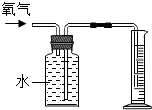 收集80mL氧气 | ||
| C. | 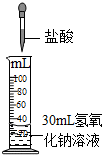 向30mL氢氧化钠溶液中滴入盐酸 | D. |  配制100g10%的氯化钾溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
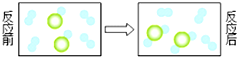
| A. | 反应前后原子种类、数目均不变 | |
| B. | 反应前后分子种类、数目均不变 | |
| C. | 反应后该密闭体系中没有单质存在 | |
| D. | 参加反应的两种分子个数比不能确定 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氢气在空气中点燃 发出黄光,放出热量 | |
| B. | 铁粉在空气中加热 剧烈燃烧、生成黑色固体 | |
| C. | 浓硫酸敞口放置 溶液的颜色、质量不变 | |
| D. | 烧碱固体放入水中 迅速溶解、溶液温度升高 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 宏观--微观--符号之间建立联系是化学学科特有的思维方式.汽车尾气是造成大气污染的主要原因之一,在汽车排气管上安装“催化转化器”便可以将汽车的尾气转化成无毒气体.如果用
宏观--微观--符号之间建立联系是化学学科特有的思维方式.汽车尾气是造成大气污染的主要原因之一,在汽车排气管上安装“催化转化器”便可以将汽车的尾气转化成无毒气体.如果用 表示碳原子,用
表示碳原子,用 表示氧原子,用
表示氧原子,用 表示氮原子,图为气体转换的微观过程,请你根据图示回答下列问题.
表示氮原子,图为气体转换的微观过程,请你根据图示回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 10g | B. | 12g | C. | 14g | D. | 16g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com