
分析 根据物质的组成分析,含有碳元素的化合物是有机物,不含有碳元素的化合物属于无机物;混合物是由不同种物质组成的,纯净物是由同种物质组成的.据此分析、写出各组中与众不同物质的化学式.
解答 解:(1)一氧化碳虽含有碳元素,但性质同无机物相似,常归到无机物类;乙炔、甲烷、尿素是含有碳元素的化合物属于有机物. 与众不同的物质是一氧化碳,化学式:CO;
(2)纯碱、碳酸钙、小苏打,属于盐;烧碱属于碱.与众不同的物质是烧碱,化学式是:NaOH;
(3)石油、碘盐、孔雀石,都属于混合物;氯酸钾属于纯净物.与众不同的物质是氯酸钾,化学式是:KClO3;
(4)菜籽油、牛油、豆油属于油脂,葡萄糖属于糖类,与众不同的物质是葡萄糖,化学式是:C6H12O6.
故答为:(1)CO;(2)NaOH;(3)KClO3;(4)C6H12O6.
点评 本题的难度不大,了解物质的组成和分类的知识是解答本题的关键.


科目:初中化学 来源: 题型:选择题
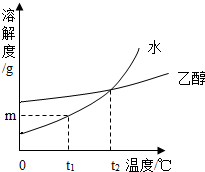 固体物质W在水、乙醇两种溶剂中的溶解度随温度变化的曲线如图所示,下列说法正确的是( )
固体物质W在水、乙醇两种溶剂中的溶解度随温度变化的曲线如图所示,下列说法正确的是( )| A. | 物质w在乙醇中的溶解度小于其在乙醇中的溶解度 | |
| B. | t2℃时,物质W溶解在水中和乙醇中的溶质质量分数一定相等 | |
| C. | t1℃时,mgW分别溶解在100g水和乙醇中,两者都达到了饱和状态 | |
| D. | 将t1℃时物质W的饱和乙醇溶液升温至t2℃,溶质质量分数不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
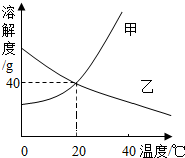 甲、乙两物质的溶解度曲线右图所示,请据图回答下列问题.(1)P点表示的意义是在20℃时,甲和乙两物质的溶解度为40g;
甲、乙两物质的溶解度曲线右图所示,请据图回答下列问题.(1)P点表示的意义是在20℃时,甲和乙两物质的溶解度为40g;查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用蒸馏水区别四氧化三铁与二氧化锰 | |
| B. | 用酚酞试液区别氯化钠溶液与稀醋酸 | |
| C. | 用加热石灰研磨的方法区别碳酸氢铵与尿素 | |
| D. | 用石蕊试液区别稀烧碱溶液与石灰水 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
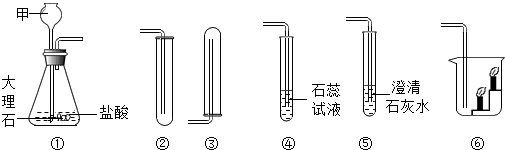
| A. | ①所示仪器甲是长颈漏斗 | B. | ④说明CO2能使石蕊试液变红 | ||
| C. | ③可用于收集和检验气体 | D. | ④⑤⑥只能验证其化学性质 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量固体于试管中,加水振荡直至完全溶解. | 不产生气泡 | 猜想I不成立. |
| ②取少量①的溶液于试管中,滴加过量的Ba(NO3)2溶液. | 产生白色沉淀 | 证明有Na2CO3存在. |
| ③取少量②的溶液于试管中,滴加酚酞试液 | 溶液变红 | 证明有NaOH存在. |
| 综合以上实验现象,说明猜想II是成立的. | ||
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
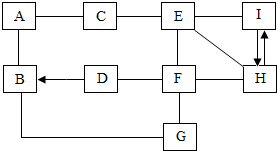 已知A~I均为初中化学常见的物质,它们相互间的关系如图所示.该图体现了化合物F四种不同的化学性质,其中B溶液呈蓝色,I是无色无味的气体,B、C分别与A反应均有不溶于稀硝酸的同种白色沉淀产生,E与F反应生成另一种不溶于稀硝酸的白色沉淀,C与E反应产生氨味气体.(“-”表示两物质间能反应,“→”表示物质间的转化关系.)
已知A~I均为初中化学常见的物质,它们相互间的关系如图所示.该图体现了化合物F四种不同的化学性质,其中B溶液呈蓝色,I是无色无味的气体,B、C分别与A反应均有不溶于稀硝酸的同种白色沉淀产生,E与F反应生成另一种不溶于稀硝酸的白色沉淀,C与E反应产生氨味气体.(“-”表示两物质间能反应,“→”表示物质间的转化关系.)查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 温度/℃ | 20 | 30 | 40 | 50 | |
| 溶解度(g/100g水) | KCl | 34.0 | 37.0 | 40.0 | 42.6 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | |
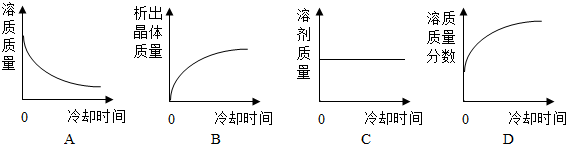
| 实验步骤 | 实验现象 | 实验结论 |
| 向不饱和的氯化钾溶液 中不断加入氯化钾固体 | 有固体不再溶解 | KCl不饱和溶液 变为饱和溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
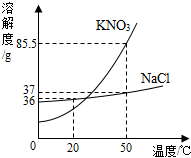 NaCl、KN03两种物质的溶液度曲线图如图所示,请回答:
NaCl、KN03两种物质的溶液度曲线图如图所示,请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com