
【题目】绿矾(FeSO4·7H2O)、硫酸亚铁铵[FeSO4·(NH4)2SO4·6H2O]是重要的化工试剂。工业上常利用机械加工行业产生的废铁屑为原料制备绿矾、硫酸亚铁铵(如下图)。

已知:
(1)废铁屑中含有FeS等杂质,FeS+H2SO4=FeSO4+H2S↑,生成的H2S气体有毒。
(2)在0~60℃时,硫酸亚铁铵的溶解度比硫酸铵、硫酸亚铁的小,冷却混合液至室温便析出硫酸亚铁铵。
(3)硫酸亚铁易被氧气氧化为硫酸铁,影响硫酸亚铁铵的等级。
请回答下列问题:
实验一:制备绿矾:
图Ⅰ中仪器①盛放的液体是_____,除了发生的反应FeS+H2SO4=FeSO4+H2S↑外,还发生的另一个反应的化学方程式是_____。广口瓶的作用是_____,烧杯中主要的反应是CuSO4+H2S=CuS↓+H2SO4,硫酸铜溶液的作用是_____;此处烧杯中的导管最好换成多孔球泡,目的是_____。
实验二:制备硫酸亚铁铵:
如图Ⅱ。实验步骤如下:
①连接仪器,_____
②制备FeSO4溶液:先关闭止水夹A,再打开止水夹_____,从分液漏斗滴入稀H2SO4至锥形瓶中。其中NaOH溶液中发生反应的化学方程式为_____,此过程中氢气的作用是_____。
③制备硫酸亚铁铵:待锥形瓶中的铁屑快反应完时,关闭止水夹_____,打开止水夹_____,不久会看到锥形瓶中的液体被压入饱和硫酸铵溶液中,放置一段时间,试剂瓶底部将结晶出硫酸亚铁铵晶体。
实验三:对所制得的硫酸亚铁铵样品进行加热
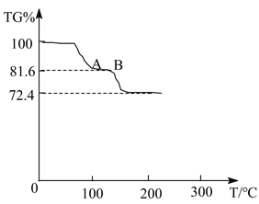
温度与TG%的关系如图所示,已知,200℃以前只有结晶水失去。[Mr(FeSO4·(NH4)2SO4·6H2O)=392],已知:TG%=![]() ×100%。
×100%。
TG%从100%降低为72.4%时,发生反应的化学方程式是_____。试计算AB段物质的化学式_____(写出计算过程)。
【答案】稀硫酸 ![]() 安全瓶(或防倒吸) 尾气处理,防止污染大气 增大接触面积,使反应更充分 检查装置的气密性 BC
安全瓶(或防倒吸) 尾气处理,防止污染大气 增大接触面积,使反应更充分 检查装置的气密性 BC ![]() 排出装置和硫酸铵溶液中的氧气 BC A
排出装置和硫酸铵溶液中的氧气 BC A ![]() FeSO4·(NH4)2SO4·2H2O
FeSO4·(NH4)2SO4·2H2O
【解析】
实验一:工业制备绿矾常用废铁屑和硫酸反应进行制取,故图Ⅰ中仪器①盛放的液体是稀硫酸;废铁屑中一定含有铁,铁和硫酸反应生成硫酸亚铁和氢气,![]() ;广口瓶作为安全瓶收集产生的硫化氢气体和氢气;烧杯中的硫酸铜溶液主要是吸收尾气H2S,防止污染大气;烧杯中的导管最好换成多孔球泡,目的是增大气体与溶液的接触面积,使反应充分进行;
;广口瓶作为安全瓶收集产生的硫化氢气体和氢气;烧杯中的硫酸铜溶液主要是吸收尾气H2S,防止污染大气;烧杯中的导管最好换成多孔球泡,目的是增大气体与溶液的接触面积,使反应充分进行;
实验二:①仪器连接好,一般都要检查装置的气密性,尤其是有气体参加或者生成的反应;
②制备FeSO4溶液先关闭止水夹A,再打开止水夹BC,是为了用产生的氢气将装置内的空气排出,因为亚铁盐容易被氧化;
废铁屑中含有FeS等杂质,硫化亚铁会与硫酸反应生成硫酸亚铁和硫化氢气体,氢氧化钠溶液就是为了吸收硫化氢气体,方程式为:![]() ;此过程中氢气的作用是排出装置和硫酸铵溶液中的氧气,因为亚铁盐容易被氧化;
;此过程中氢气的作用是排出装置和硫酸铵溶液中的氧气,因为亚铁盐容易被氧化;
③制备硫酸亚铁铵:待锥形瓶中的铁屑快反应完时,关闭止水夹BC,打开止水夹A,产生的氢气使锥形瓶中压强增大,将硫酸亚铁压入左边的瓶中,使之反应;
实验三:通过分析可知,对硫酸亚铁铵[FeSO4·(NH4)2SO4·6H2O]样品进行加热到100℃时,首先是固体表面的分子水蒸发得到硫酸亚铁铵[FeSO4·(NH4)2SO4·6H2O],这一步是物理变化,继续加热到100-200℃时,已知200℃以前只有结晶水失去,因此硫酸亚铁铵[FeSO4·(NH4)2SO4·6H2O]中的结晶水开始脱去,这一步是化学变化.
所以TG%从100%降低为72.4%时,发生反应的化学方程式是:![]() ;
;
假设硫酸亚铁铵晶体质量是392克,AB段物质的化学式为FeSO4·(NH4)2SO4·xH2O;
加热到200℃时,失去结晶水,剩下的硫酸亚铁铵质量为:![]() ;
;
由关系图可知AB段的TG%=81.6%,即![]() ,m水=35.872g,则
,m水=35.872g,则![]() ,所以AB段物质的化学式为FeSO4·(NH4)2SO4·2H2O。
,所以AB段物质的化学式为FeSO4·(NH4)2SO4·2H2O。


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:初中化学 来源: 题型:
【题目】某化学兴趣小组的同学来到实验室准备做制取气体的实验。如图是实验室制取气体的常用装置:

(1)写出图中标号仪器的名称:a_____;b_____。
(2)实验室常用B装置作为制取氧气的发生装置,写出反应的化学方程式_____。
(3)小组同学想用大理石和稀盐酸反应制取CO2,则他选择B装置作气体发生装置的优点是_____,若要制得干燥的CO2,还应该将气体通入_____(填装置编号,下同)装置。
(4)甲烷是一种无色、无味、难溶于水、密度小于空气的气体,实验室常用加热无水醋酸钠和碱石灰固体混合物的方法制取甲烷,则选用的发生装置和收集装置分别为_____、_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出。生成的是什么气体呢?同学们决定进行探究。探究前老师提示,该反应生成的气体只有一种。
(提出猜想)放出的气体可能是SO2、O2、H2,提出猜想的依据是______。
(查阅资料)SO2易溶于水,化学性质与二氧化碳有相似之处,它能使澄清石灰水变浑浊,生成CaSO3。
(方案设计)依据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是O2,则检验方法是______。
(2)乙同学认为是SO2,则需将放出的气体通入澄清石灰水中,看澄清石灰水是否变浑浊。写出SO2与Ca(OH)2反应的化学方程式______。
(3)实验小组同学在老师的指导下合作设计了如下组合实验方案(浓H2SO4用于干燥气体),排除和验证猜想的气体。
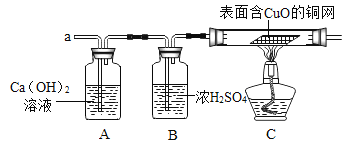
(实验探究)实验开始时,先将收集到的气体从a通入一段时间后,再点燃C处酒精灯;这样操作的目的是______。
实验过程中发现A装置中溶液不变浑浊,C装置中表面含CuO的铜网由黑色变为光亮的红色;
C装置中发生反应的化学方程式______。
结论:铁粉与硫酸铜溶液反应时,产生的气体是______。
(思维拓展)由上述实验可以推出,硫酸铜溶液中可能含有______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验不能达到目的的是( )
|
|
|
|
A.探究铁、铝、铜的活动性强弱 | B.探究CO2是否与水发生了反应 | C.探究影响反应速率的因素 | D.探究温度对物质溶解速率的影响 |
A. AB. BC. CD. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是某反应的微观示意图,关于该反应的说法中,正确的是
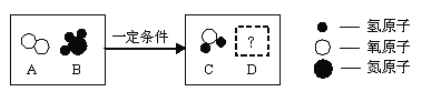
A. 反应前后,分子种类不变B. 若D为单质,则C、D质量比为9:14
C. 该反应一定为置换反应D. 该反应中,一定有元素化合价改变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】中考实验操作考查中,小明抽到“二氧化碳的制取”,如图(a﹣g)是提供的实验仪器。根据要求回答问题:
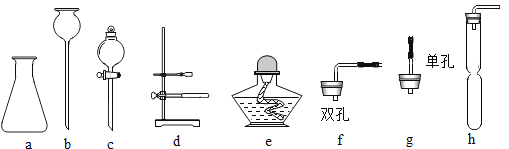
(1)仪器a的名称为_____。小明选用仪器a、g组装了简易发生装置,反应原理用化学方程式表示为_____,收集装置需要一根直角导管、毛玻璃片和_____(填仪器名称)。
(2)若选用a、c、f组装发生装置,与简易装置比较,其优点是_____。
(3)为确认残留液中是否有盐酸,小明设计的方案中错误的是_____(填字母序号)。
A 取样,加入少量锌粒,观察是否有气泡产生
B 取样,滴加少量碳酸钠溶液,观察是否有气泡产生
C 取样,滴加少量硝酸银溶液,观察是否产生沉淀
D 取样,滴加少量紫色石蕊溶液,观察溶液是否变红
(4)小明回家后寻找身边的物品做家庭实验。用鸡蛋壳代替石灰石,用_____代替稀盐酸。并找到一种“吸吸冻”的软塑料瓶,用橡皮塞和导管组装了如h图的发生装置,该装置可以控制反应的发生与停止。他先将盐酸替代液吸入到细腰的下方,后将碎鸡蛋壳放到细腰的上方,需要产生气体时的操作方法为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验设计不能达到实验目的的是
选项 | A | B | C | D |
实验 目的 | 验证质量守恒定律 | 验证铁丝能在 氧气中燃烧 | 验证与氧气接触是燃烧的条件之一 | 鉴别NaCl、NaOH和 稀盐酸三种溶液 |
实验 方案 |
|
|
|
|
A. AB. BC. CD. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下图回答问题。

(1)图中仪器a的名称是__________。
(2)用A与D相连可制取的一种气体是 ________ ,该反应的化学方程式为_____________________。
(3)小明将B与C相连,用高锰酸钾制取氧气。实验操作有:a.停止加热b.固定试管c.将导管从水槽中取出d.装药品和放棉花e.加热,收集氧气。上述过程中缺少的一步操作是_______________,将该操作编号为f,则正确的操作顺序是 _____________________。
(4)查阅资料:在相同条件下,氨气(NH3)的密度比空气小,且易溶于水,其水溶液称为氨水;加热氯化铵和氢氧化钙固体混合物可制取氨气。根据所查资料,制取氨气应选择的装置是_______(填序号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com