
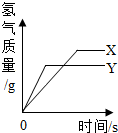
 将等质量的X和Y两种金属粉末,分别放入相同质量分数的足量稀盐酸中,反应生成H2的质量与反应时间的关系如图所示,据图回答
将等质量的X和Y两种金属粉末,分别放入相同质量分数的足量稀盐酸中,反应生成H2的质量与反应时间的关系如图所示,据图回答分析 (1)由图示信息可知谁先到达最高点,谁活泼反应的速度快;
(2)根据等质量的铁与锌与足量酸反应生成氢气的多少考虑.
(3)根据(1)(2)的分析,可以推测金属X、Y.
解答 解:(1)金属活动性越强,反应速度越快,用的时间就越短,所以最先到达最高点的说明该金属活泼
,故X、Y两种金属的活动性顺序为Y>X;
(2)由于金属X、Y在与盐酸反应时得到的盐溶液中金属元素的化合价都是+2价,化合价相同时相对原子质量越小产生氢气质量越多,相对原子质量越大产生氢气质量越少,所以X产生氢气比Y多,所以Y的相对原子质量较大;
(3)根据(1)(2)的分析,可以推测X、Y可能是Fe与Zn.
故答案为:
(1)Y>X,反应速度越快,用的时间就越短.
(2)Y.(3)B.
点评 解答本题关键是要知道化合价相同时相对原子质量越小产生氢气质量越多,相对原子质量越大产生氢气质量越少;最先到达最高点的金属反应速度最快.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaOH 纯碱 氢氧化钠 | B. | CaCO3 石灰石 碳酸钙 | ||
| C. | CaO 生石灰 氧化钙 | D. | CO2 干冰 二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | HNO3,NH3•H2O,CuSO4 | B. | KNO3,NaOH,HCl | ||
| C. | H2SO4,Na2CO3,KOH | D. | Ca(OH)2,HCl,NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物 质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 4 | 18 | 10 | 1 |
| 反应后质量(g) | 待测 | 2 | 21 | 10 |
| A. | 该变化的基本反应类型是化合反应 | B. | 参加反应的甲、丙的质量比为2:11 | ||
| C. | 丙、丁是反应物 | D. | 甲反应后的质量为0g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com