
���й���ͼ���������ȷ����

�� �� �� ��
A��ͼ�ٱ�ʾ��������ʯ��ˮ�м���һ���������ƣ����ָ�������
B��ͼ�ڱ�ʾ�Ѳ����⼣������Ͷ�뵽������ϡ������
C��ͼ�۱�ʾ������������Һ�м��������ˮ
D��ͼ�ܱ�ʾ�������������Һ��������ˮ��
B �������� ��������� ������ͼ���⣬����һ��Ҫ�Ѻ����ꡢ����������ʾ�����������Ȼ��ץס�����㣨����ʼ�㡢ת�۵㡢�յ㣩һ���ƣ�A������������ʯ��ˮ�м���һ���������ƣ���������������ˮ��Ӧ������������Һ�е�ˮ�ּ��٣�������Ȼ������������������Ӧ���٣�����B���Ѳ����⼣������Ͷ�뵽������ϡ�����У��տ�ʼ������ϡ���ᷴӦ��Fe2O3+3H2SO4==Fe2(SO4)3+3H2O...
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��������2018����꼶5���¿���ѧ�Ծ� ���ͣ������
�������ڹ�������������������ʱ��������Ҫ�����á�
(1)75���ľƾ�����Ϊ��ҽ�þƾ�����������ɱ�����������е��ܼ���_______��
(2)ҽ���ϳ���3���Ĺ���������Һ�����˿�����������ʱ�����������ݲ�����������һ�����ԭ����_____________(�û�ѧ����ʽ��ʾ)��
ˮ 2H2O2��2H2O+O2�� ����������1��75%�ľƾ�����Ϊ��ҽ�þƾ��������Ǿƾ���ˮ��Һ�����е��ܼ���ˮ�� ��2����3%�Ĺ���������Һ�����˿�����ʱ�����������ݲ���������ΪH2O2�ֽ������O2��ͬʱ������ˮ����ѧ����ʽΪ��2H2O2=2H2O+O2�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ�������彭����2018����꼶��ģ��ѧ�Ծ� ���ͣ��ƶ���
A-F�dz��л�ѧ������6�����ʣ��ֱ��� C��H��O��Cl��Ca�е�һ�ֻ���Ԫ����ɣ���֪A��B��C��D �Dz�ͬ�����������C �Ǵ���ʯ����Ҫ�ɷ֣�E ��һ�ֿ�ȼ�����塣��Щ����֮�����ϵ����ͼ��ʾ��ͼ�С�������ʾ�����Ӧ��ͼ�С�������ʾת����ϵ��(���ַ�Ӧ������P��Ӧ��������ȥ)
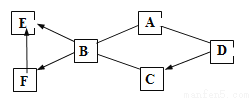
(1)E�Ļ�ѧʽ��_______��
(2)B �� F��Ӧ�Ļ�ѧ����ʽ��_______��(����дһ��)
(3)�о�A��ũҵ�����е�һ����;_______��
H2 HCl+NaOH=NaCl+H2O�� ���������������Ʋ�����Һ�� ��������������Ŀ����������ͼ����Ϣ����֪A��B��C��D�Dz�ͬ�������ʣ�C�Ǵ���ʯ����Ҫ�ɷ֣����C��̼��ƣ�D��G���Ԫ����ͬ��E��һ�ֿ�ȼ�����壬H��������һ����̬���ʣ�������̼��һ����̼���Ԫ����ͬ�����Ҷ�����̼��̼�ڸ��µ�����������һ����̼�����D�Ƕ�����̼��G��һ����̼��̼���������ȼ�����ɶ�����̼�������ȼ��...�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ�������п��Եڶ���ģ�⿼�Ի�ѧ�Ծ� ���ͣ�ʵ����
��ͼ��ʵ������ȡ����IJ���װ�á�

��1��д��һ����Aװ����ȡ����Ļ�ѧ����ʽ_______��
��2��B��Cװ�þ�����ȡ���壬����Cװ�õ��ŵ���ʲô��_______
��3��������ˮ���ռ���������������D����ƿ��װ��ˮ���ٴ�________��ѡ�a����b��������ͨ��������
2KMnO4 K2 MnO4 + MnO2 + O2 �� ( ��2KClO32KCl + 3O2 ��) ����ʱ���Ʒ�Ӧ�ķ�����ֹͣ b ��������(1).ѡ����װ���迼���������ǣ���Ӧ���״̬�ͷ�Ӧ���������ȹ�����ȡ���壬����װ��ΪA��������ط�������ط���ȡ����������Aװ�ã���Ӧ����ʽΪ��2KMnO4 K2 MnO4 + MnO2 + O2 �� ( ��2KClO3 2KCl + 3O2 ��...�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ�������п��Եڶ���ģ�⿼�Ի�ѧ�Ծ� ���ͣ������
��ͼ��ij��Һƿ��ǩ�ϵIJ������ݡ�����̼Ԫ�ص���������Ϊ_________��Ҫ��10g������������Һϡ�ͳ�2%����Һ����Ҫˮ������Ϊ____________g��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ�������п��Եڶ���ģ�⿼�Ի�ѧ�Ծ� ���ͣ���ѡ��
���и��������У����ɷ��ӹ��ɵ�һ����
A. ��ͽ��ʯ B. �����Ȼ��� C. �ɱ�������ͭ D. ˮ�Ͱ���
D ��������A. ��ͽ��ʯ ����ԭ��ֱ�ӹ��ɣ� B. ���ɹ�ԭ��ֱ�ӹ��ɣ��Ȼ��� �������Ӻ�������ֱ�ӹ��ɣ� C. �ɱ��ǹ��������̼���׳ƣ��ɶ�����̼����ֱ�ӹ��ɣ�����ͭ ����ͭ���Ӻ���������ӹ��ɣ� D. ˮ����ˮ���ӹ��ɣ��������ɰ������ӹ��ɣ�ѡD�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡׯ����2017-2018ѧ��ڶ�ѧ�ھ��꼶��ѧ�����Ծ� ���ͣ�������
ij����(Na2CO3)��Ʒ�к��������Ȼ��ơ�Ϊ�ⶨ��Ʒ��̼���Ƶ���������,�ֳ�ȡ����Ʒ11g,���뵽ʢ��50gϡ������ձ���,ǡ����ȫ��Ӧ,���Ƶ��ձ�����Һ������Ϊ56.6g��(��ܰ��ʾ��Na2CO3+2HC1�T2NaC1+H2O+CO2��)���㣺
�ٷ�Ӧ����CO2�����������___g��
�ڴ�����Ʒ��̼���Ƶ���������_____________g��
����������ձ��е���Һ���ɣ��ɵ�________g�Ȼ��ƹ���?
4.4 96.4% 12.1g ���������ٸ��������غ㶨��֪����Ӧ����CO2�����������11g��50g��56.6g��4.4g�� �ڽ���贿����Ʒ��̼���Ƶ���������Ϊx�������Ȼ���Ϊy Na2CO3+2HC1�T2NaC1+H2O+CO2�� 106 `117 44 11g��x y 4.4g ����x��96.4%�� ����y��11.7g�� ����������ձ��е���...�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡׯ����2017-2018ѧ��ڶ�ѧ�ھ��꼶��ѧ�����Ծ� ���ͣ���ѡ��
2016��4��22�գ��й�ǩ���ˡ�����Э�������й�����������ʵ������Э������������ɫ��չ�ľٴ룬Ӯ���˹������Ļ������ۣ����������У���������ɫ��չ������ǣ� ��
A������������� B������С��ո�
C���ܾ�һ���Կ��� D����չ̫���ܵ��
B �������� �������������С��ոѣ�����������к�������̳�������Ⱦ�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ��β����ͤ��У����СƬ��2018����꼶��ѧ�ڵ�һ���¿���ѧ�Ծ� ���ͣ�������
ȡ100gһ������������Ba(OH)2��Һ���ձ��У�������������Ϊ20%��H2SO4��Һ��ʵ������У���Һ��pH�����H2SO4��Һ��������ϵ��ͼ��ʾ�������Ba(OH)2��Һ�����ʵ������������� ��Ӧ�ķ���ʽΪ��Ba(OH)2 + H2SO4 ==== BaSO4��+ 2H2O��

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com