
| 选项 | 分类 | 举例 |
| A | 常见合金 | 生铁、不锈钢、青铜 |
| B | 常见酸 | 盐酸、硫酸、醋酸 |
| C | 常见碱 | 熟石灰 纯碱 氨水 |
| D | 常见干燥剂 | 浓硫酸、生石灰、烧碱 |
| A. | A | B. | B | C. | C | D. | D |
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 淀粉没有甜味,因此不属于糖类 | B. | 肥皂水可以区别硬水和软水 | ||
| C. | 生铁和钢都是铁的合金 | D. | 钢筋混凝土是复合材料 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 除去NaHCO3溶液中混有的Na2CO3,可以通入适量的二氧化碳 | |
| B. | 除去BaCl2溶液中的少量HCl,可以加入过量的BaCO3,然后过滤 | |
| C. | 某溶液中滴加稀盐酸,有气泡生成,将气体通入澄清石灰水变浑浊,该溶液中一定是碳酸根离子 | |
| D. | 在久置的某氢氧化钠溶液中滴加酚酞,溶液变红;再加入过量的氯化钡溶液,有白色沉淀生成,同时溶液变为无色.说明该氢氧化钠溶液已经部分变质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 铜及其化合物一般都具有特征的颜色,例如Cu、Cu2O呈红色,CuO呈黑色,CuSO4•5H2O呈蓝色等.研究性学习小组甲为检测实验室用H2还原CuO所得红色固体中是否含有Cu2O进行了认真的探究.
铜及其化合物一般都具有特征的颜色,例如Cu、Cu2O呈红色,CuO呈黑色,CuSO4•5H2O呈蓝色等.研究性学习小组甲为检测实验室用H2还原CuO所得红色固体中是否含有Cu2O进行了认真的探究.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
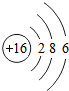 ⑤
⑤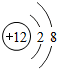
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 实验编号 | 选用金属 (均取2g) | 盐酸质量分数 (均取50mL) | 每分钟产生氢气的体积/mL | |||||
| 1分钟 | 1~2分钟 | 2~3 分钟 | 3~4分钟 | 4~5分钟 | 前5分钟共收集气体 | |||
| 1 | 锌片 | 15% | 2.9 | 16.9 | 11.9 | 9.2 | 7.6 | 48.5 |
| 2 | 锌片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 同一物质:火碱,纯碱,苛性钠 | B. | 复合肥料:氯化铵、磷矿粉、硝酸钾 | ||
| C. | 化石燃料:煤、石油、天然气 | D. | 混合物:氢气、石灰石、空气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com