����Դ�Ŀ��������ǵ���ȫ���һ���ش��о����⣬��չ����Դ���Ź�����ǰ�������������õ��ˮ�ķ�����ȡ������������Դ���ش��������⣺
��1���õ��ˮ�ķ�����ȡ������ʵ������______����______�ܵ�ת����
��2������������ֵΪ1.43��108J/kg�����9.9gˮ������������ȫȼ�շų���������______��
��3����ʹ����Ȼ����ȼ����ȣ���������ȼ�ϳ��˷��������⣬������˵��һ���ŵ㣺______��
��4������������Ҫ�ɻ�ѧ�仯��������
A�����ٶ�ͨ�緢������������������ B�����ͨ�緢���Ĺ�
C��ˮ��վ����ˮ�������ĵ��ܡ����� D��Һ��ʯ����ȼ�շų���������
�⣺��1���ڵ��ˮʱ������ת��Ϊ��ѧ�������������У���ת��Ϊ���ܣ�
��2���裺���9.9gˮ����������������ΪX
2H
2O

2H
2��+O
2��
36 4
9.9g X
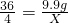
X=1.1g
1.1g��10
-3kg/g��1.43��10
8J/kg=1.573��10
5J��
��3��������Ϊȼ���������ŵ㣺ȼ�շ��ȶࡢ����������Ⱦ��ˮ������ˮ��ȡ��ȼ��������ˮ����������
��4��A�����ٶ�ͨ�緢���������ǵ���ת��Ϊ���ܣ�û�з�����ѧ�仯�����Դ���B�����ͨ�緢���Ĺ��ǵ���ת��Ϊ���ܣ�û�з�����ѧ�仯�����Դ���C��ˮ��վ����ˮ�������ĵ�����ˮ������ת��Ϊ���ܣ�û�з�����ѧ�仯�����Դ��� D��Һ��ʯ����ȼ�շų��������ǻ�ѧ��ת��Ϊ���ܣ���ͨ����ѧ�仯�ų����ܵģ�������ȷ��
�ʴ�Ϊ��
��1���磻�⣻
��2��1.573��10
5J��
��3��ȼ�ղ����Dz���Ⱦ������ˮ�������������
��4��D��
��������1�����ݵ��ˮ��Ӧ�е������仯�ش�
��2�����ݵ��ˮ�Ļ�ѧ����ʽ������9.9gˮ�������������������ٸ�����������ֵ������ȫȼ�շų���������
��3������������Ϊȼ�ϵ������ŵ�ش�
��4�����������仯�е������仯����жϣ�
��������Դ����Ϣ�����ϡ������ǵ��������Ĵ���Ҫ���⣬����ԴΣ���������صĽ��죬����������ȵ㣬Ҳ�ǻ�ѧ������ȵ㣬��Ҫ������Դ�ķ��ࡢ��Դʹ�öԻ�����Ӱ�졢����Դ�����ļ�����ǰ���ȣ�

 2H2��+O2��
2H2��+O2��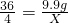



 ���ž��õķ�չ����Դ�뻷����Ϊ���������ע�����⣮
���ž��õķ�չ����Դ�뻷����Ϊ���������ע�����⣮