
| A. | 氨气液化是物理变化 | B. | 液氨具有可燃性,可用作燃料 | ||
| C. | X的化学式为N2 | D. | 该反应属于复分解反应 |
分析 由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
解答 解:A、氨气液化是物理变化,该选项说法正确;
B、液氨具有可燃性,可用作燃料,该选项说法正确;
C、由4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2X+6H2O可知,
反应前氮原子是4个,反应后应该是4个,包含在2X中;
反应前氢原子是12个,反应后是12个;
反应前氧原子是6个,反应后是6个;
由分析可知,每个X中含有2个氮原子,是氮气,X的化学式N2,该选项说法正确;
D、因为4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O,则该反应属于置换反应,而非复分解反应,故该选项说法不正确.
故选:D.
点评 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:初中化学 来源: 题型:解答题
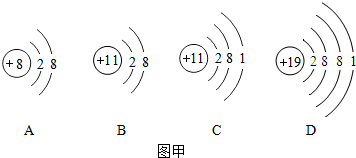
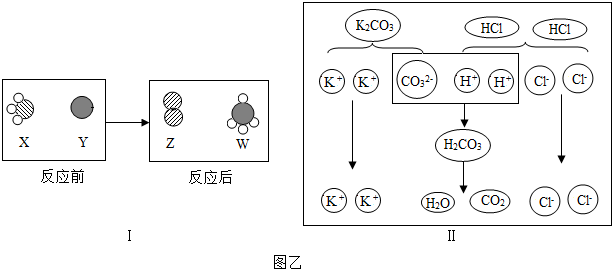
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 在一定质量的甲溶液中逐渐加入乙物质至过量,反应过程中溶液的总质量与加入乙的质量的关系与如图曲线相符的是 ( )
在一定质量的甲溶液中逐渐加入乙物质至过量,反应过程中溶液的总质量与加入乙的质量的关系与如图曲线相符的是 ( )| 序号 | 甲 | 乙 |
| A | CuSO4溶液 | 铁粉 |
| B | H2SO4溶液 | 锌粒 |
| C | HCl溶液 | NaOH溶液 |
| D | CaCl2溶液 | Na2CO3溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 胃液中的胃酸(0.2%~0.4%的盐酸),可以杀死食物里的细菌,确保胃和肠道的安全,同时增加胃蛋白酶的活性,帮助消化,正常人胃液每日需要盐酸溶质质量约为6.5g~7.3g,某患者每日分泌盐酸溶质质量为9.0g,为治疗胃酸过多需服用图所示抑酸剂,请计算并回答:
胃液中的胃酸(0.2%~0.4%的盐酸),可以杀死食物里的细菌,确保胃和肠道的安全,同时增加胃蛋白酶的活性,帮助消化,正常人胃液每日需要盐酸溶质质量约为6.5g~7.3g,某患者每日分泌盐酸溶质质量为9.0g,为治疗胃酸过多需服用图所示抑酸剂,请计算并回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | MgCl2•6H2O | B. | MgCl2•5H2O | C. | MgCl2•3H2O | D. | MgCl2•2H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
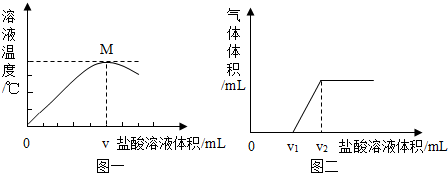
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
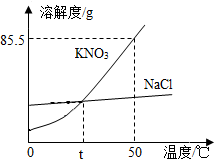 如图为KNO3、NaCl的溶解度曲线.
如图为KNO3、NaCl的溶解度曲线.查看答案和解析>>
科目:初中化学 来源: 题型:推断题
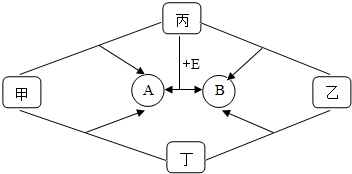 如图是初中化学中常见物质间的转化关系.
如图是初中化学中常见物质间的转化关系.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com