
| A. | 都能确定 | B. | 都不能确定 | C. | 只有①②能确定 | D. | 只有⑤不能确定 |
分析 根据所给物质的化学式进行分析,可以发现,在这两种物质中,铁元素与硫元素的原子个数比都为1:1,也就是铁元素和硫元素的质量比是定值,等于56:32=7:4,根据氧元素的质量分数来确定硫元素的质量分数以及钠元素和钙元素的质量分数.
解答 解:因为在FeSO4和FeS中,铁元素和硫元素的质量比是定值,等于56:32=7:4;由于元素质量比与元素质量分数之比是相等的,设铁元素的质量分数为x,则
7:4=x:32%,解得x=56%,即铁元素的质量分数为56%;氧元素的质量分数=1-32%-56%=12%;
假设混合物的质量为100g,设FeSO4的质量为x,则FeS的质量为100g-x,
FeSO4中硫元素的质量分数为:$\frac{32}{56+32+64}×100%$≈21.1%;
FeS中氧元素的质量分数为:$\frac{32}{56+32}×100%$≈36.4%.
∴21.1%x+36.4%×(100g-x)=100g×32%,
x=28.5g
则FeS的质量为:100g-28.5g=71.5g.
则FeSO4和FeS的质量比为:28.5g:71.5g=57:143;
混合物中FeSO4的质量分数为:$\frac{28.5g}{100g}×100%$=28.5%;
因为题目未告知混合物的总质量,因此不能确FeS的具体质量.
故选D.
点评 本题主要考查学生灵活运用元素的质量分数公式进行计算的能力.难度稍大.


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
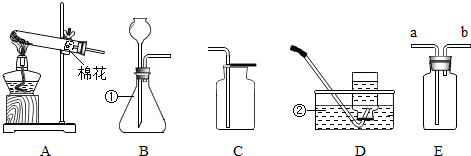
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 绿原酸由碳元素、氢元素、氧元素组成的 | |
| B. | 该绿原酸中氢元素的质量分数最小 | |
| C. | 绿原酸分子中含有16个碳原子、18个氢原子、9个氧原子 | |
| D. | 绿原酸(C16H18O9)相对分子质量为354 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 吸入雾霾、PM2.5等对人体健康没有危害 | |
| B. | 电解水实验中正极和负极产生的两种气体质量比为1:2 | |
| C. | 呼出的气体中含量最多的气体是二氧化碳 | |
| D. | 在用红磷测定空气中氧气的体积分数时,充分反应后,需将装置冷却至室温再打开弹簧夹读数,否则测量结果偏低 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验编号 | 实验药品 | 分解温度(℃) |
| ① | 氯酸钾 | 580 |
| ② | 氯酸钾、二氧化锰(质量比1:1) | 未测 |
| ③ | 氯酸钾、氧化铜(质量比l:1) | 370 |
| ④ | 氯酸钾、氧化铁(质量比1:1) | 390 |
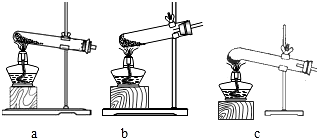
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 核电荷数为3~18的元素的原子结构示意图等信息如下,请回答下列问题:
核电荷数为3~18的元素的原子结构示意图等信息如下,请回答下列问题:| 族 周期 | I A | II A | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
| 3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com