
试用如图所示装置设计一个实验,验证煤气中一定含有H2O、CO2、CO、H2四种气体(假设每步操作中,参加反应的气体都完全反应或被完全吸收).要求验证过程不逸出毒气.
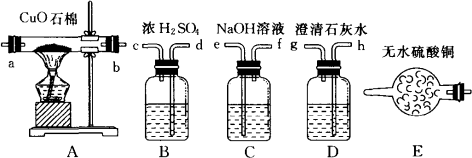
(1)验证CO2存在的操作是:将煤气通过________装置(填序号),确证CO2存在的现象是________.
(2)验证H2O存在的操作是:将煤气通过________装置(填序号),确证H2O存在的现象是________.
(3)某同学用下列操作来验证CO、H2:将煤气依次通过e、f接d、c接a、b接h、g接i.那么该学生能否验证H2存在,为什么?________.能否验证CO存在,为什么?________.
|
答案:(1)D;澄清的石灰水变浑浊 (2)E;无水硫酸铜由白色变为蓝色 (3)不能,因CO和H2转化为CO2和H2O后先通过D装置,气流会从D中带出水;能,原有的CO2已在气流通过C装置时除尽,使D中澄清石灰水变浑浊的CO2气体,只能是由CO与CuO反应时生成的 分析:这是一道鉴别气体的创新应用题.H2O要用CuSO4来验证,CO2要通过Ca(OH)2的水溶液来验证,CO和H2要先转化为CO2和水后间接验证.因此,验证的过程是:验证H2O→验证CO2→除尽CO2→干燥CO和H2→转化→验证生成的H2→验证生成的CO2→尾气处理(本题已假设完全反应,不用做尾气处理).导气管的连接应按气流方向“长进短出”. |


科目:初中化学 来源: 题型:
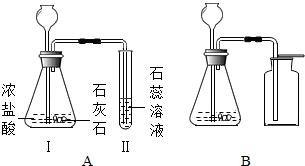
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
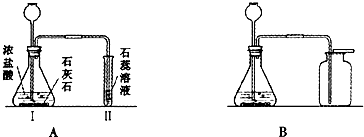
查看答案和解析>>
科目:初中化学 来源:2007-2008学年江苏省苏州市昆山市张浦中学中考化学一模试卷(解析版) 题型:解答题
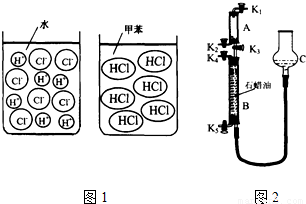
| 实验内容 | 实验现象 | 解释与结论 |
| 测定导电性 | 氯化氢的水溶液:导电性良好 | 氯化氢的水溶液中有自由移动的离子 |
| 氯化氢的甲苯溶液:不导电 | 氯化氢的甲苯溶液没有自由移动的离子 | |
| 与镁作用 | 氯化氢的水溶液:①______ | 化学方程式: ②______ |
| 氯化氢的甲苯溶液:没有明显现象 | 氯化氢的甲苯溶液没有解离出氢离子 | |
| 与固态碳酸钠作用 | 氯化氢的水溶液:产生气泡 | 化学方程式: ③______ |
| 氯化氢的甲苯溶液:④______ | 氯化氢的甲苯溶液没有解离出氢离子 |
查看答案和解析>>
科目:初中化学 来源:2007年江苏省南京市中考化学试卷(解析版) 题型:解答题

| 实验内容 | 实验现象 | 解释与结论 |
| 测定导电性 | 氯化氢的水溶液:导电性良好 | 氯化氢的水溶液中有自由移动的离子 |
| 氯化氢的甲苯溶液:不导电 | 氯化氢的甲苯溶液没有自由移动的离子 | |
| 与镁作用 | 氯化氢的水溶液:①______ | 化学方程式: ②______ |
| 氯化氢的甲苯溶液:没有明显现象 | 氯化氢的甲苯溶液没有解离出氢离子 | |
| 与固态碳酸钠作用 | 氯化氢的水溶液:产生气泡 | 化学方程式: ③______ |
| 氯化氢的甲苯溶液:④______ | 氯化氢的甲苯溶液没有解离出氢离子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com