
【题目】A-G是初中化学常见的7种物质,它们有如图所示的转化关系。
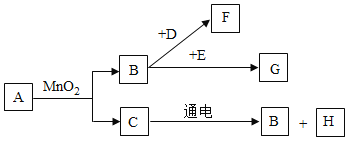
已知A、C是无色液体,B、F、G是无色气体,其中大量排放F会引起温室效应,D是黑色固体,E在纯净的B中燃烧发出明亮的蓝紫色火焰。
(1)请与出下列物质的名称: A_____;G_____;H_____;
(2)请写出下列变化的文字或符号表达式:
①C→B+H_____;
②A→B+C_____;
【答案】过氧化氢 二氧化硫 氢气 ![]()
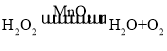
【解析】
根据大量排放F会引起温室效应,所以F就是二氧化碳;E在纯净的B中燃烧发出明亮的蓝紫色火焰,所以E就是硫,B就是氧气;C通电会生成氧气,所以C就是水,H就是氢气;A和二氧化锰会生成水和氧气,所以A就是双氧水;根据D是黑色固体,氧气和D会生成二氧化碳,所以D就是碳;氧气和硫会生成二氧化硫,所以G就是二氧化硫,将推出的物质进行验证即可。
(1)根据分析可知,下列物质的名称:A过氧化氢;G二氧化硫;H氢气;
(2)①根据分析知,C是水,在通电条件下生成氧气和氢气,反应的文字表达式为:![]() ,符号表达式为:
,符号表达式为:![]() ;
;
②根据分析知,A是过氧化氢,在二氧化锰作催化剂时分解生成水和氧气,反应的文字表达式为:![]() ,符号表达式为:
,符号表达式为: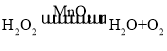 。
。


科目:初中化学 来源: 题型:
【题目】在高温条件下,A、B两种物质可以发生化学反应生成C和D.反应前后分子种类变化的微观示意图如图所示.在这个化学反应中,以下叙述正确的是 ( )
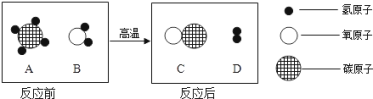
A. 该反应是化合反应 B. 物质B的相对分子质量是16
C. 生成C和D的质量比是14:3 D. 生成C和D的微粒个数比1:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小滨同学为了测定某珍珠粉中钙元素的质量分数,称取12.5g珍珠粉样品,进行四次高温煅烧、冷却、称量剩余固体的重复操作(杂质不参加反应),记录数据如下:
操作次序 | 第一次 | 第二次 | 第三次 | 第四次 |
剩余固体质量/g | 10.8 | 9.6 | 8.1 | 8.1 |
(1)完全反应后生成二氧化碳的质量为________________________ g。
(2)求该珍珠粉中碳酸钙的质量分数___________________。
(3)求该珍珠粉中钙元素的质量分数___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文(原文作者:段翰英等)。
我国制作泡菜的历史悠久。制作泡菜是把新鲜蔬菜泡在低浓度的盐水里,经发酵而成。泡菜品种繁多、风味独特、口感鲜脆。
蔬菜中含有硝酸盐。硝酸盐对人体无直接危害,但转化成亚硝酸盐后,就会产生危害。亚硝酸盐[如亚硝酸钠(![]() )]与胃酸(主要成分是盐酸)反应,产生亚硝酸(
)]与胃酸(主要成分是盐酸)反应,产生亚硝酸(![]() )和氯化物(如
)和氯化物(如![]() )。亚硝酸不稳定,产生的二氧化氮进入血液与血红蛋白结合,导致中毒。
)。亚硝酸不稳定,产生的二氧化氮进入血液与血红蛋白结合,导致中毒。
泡菜中含亚硝酸盐吗?含量有多少?含量受什么因素影响呢?
经实验测定发现,食盐水浓度和泡制时间对泡菜中亚硝酸盐含量有一定影响。下图为室温下,食盐水浓度和泡制时间与芹菜泡制过程中亚硝酸盐含量的关系。

用不同的蔬菜进行测定,变化趋势与芹菜相似。
实验表明,发酵温度对泡菜中亚硝酸盐的生成量及生成时间也具有明显的影响。泡菜发酵过程中,泡制温度较高时,亚硝酸盐含量最大值出现的早,且数值低。这与温度较高有利于乳酸菌的繁殖有关。
实验还表明,泡制过程中添加姜汁和维生素C,都能有效地减少亚硝酸盐的生成。
现代医学证明,泡菜中的乳酸和乳酸菌对人体健康有益,具有抑制肠道中的腐败菌生长、降低胆固醇等保健作用。但是,有些泡菜盐分或糖分过高,对高血压和糖尿病等慢性病患者不利。另外,泡制过程也会造成某些营养素的流失。(有删改)
依据文章内容,回答下列问题。
(1)泡菜中的亚硝酸盐是由__________转化生成的。
(2)室温下,用芹菜制作的泡菜,最佳食用时间是__________(填字母序号,下同)。
A.泡制2-3天 B.泡制5-6天 C.泡制12天后
(3)下列关于制作泡菜的说法中,合理的是__________。
A.最好加入一些姜汁 B.最好在较低温度下泡制
C.最好加入一些富含维生素C的水果
D.最佳食用期的泡菜中亚硝酸盐的含量与泡制时的食盐水浓度无关
(4)请你为喜欢吃泡菜的人提一条食用泡菜的建议:__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水与我们的生活密切相关,请你回答下列问题:
(1)淡水资源有限,我们需要节约用水。下图中表示节水标志的是_____(填字母)。
(2)自然界中的淡水需要净化才能为我们使用的自来水。净化过程中可以通过_____操作除去水中的不溶物;利用活性炭,不仅可以除去不溶性杂质,还可以_____。
(3)水的硬度过大会影响生产和生活,生活中我们可以利用_____来鉴别硬水和软水,然后利用_____的方法降低水的硬度。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定某黄铜(铜锌合金)样品中铜的含量,某化学活动小组分三次进行实验,实验数据如表,请回答下列问题:
所取药品 | 第一次 | 第二次 | 第三次 |
黄铜样品质量 | 12g | 10g | 10g |
烧杯+稀盐酸质量 | 150g | 150g | 160g |
充分反应后,烧杯+剩余物质质量 | 161.8g | 159.8g | 169.8g |
(1)第_______次实验中,稀盐酸和样品恰好完全反应。
(2)黄铜样品中铜的质量分数是多少_______?(写出计算过程)
(3)第三次实验充分反应后所得溶液中的溶质为________________(写化学式)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国科学家研究出碳化钼(Mo2C)负载金原子(Au)组成的高效催化体系,使水煤气中的CO和H2O在120℃下发生反应,反应微观模型如下图所示。
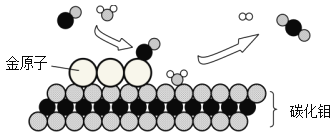
(1)反应微观模型中,“”表示_____原子,“ ![]() ”表示____________分子。
”表示____________分子。
(2)该反应过程中:
①构成催化剂的各原子__________(填“有”或“没有”)变化。
②金原子对____________(填“CO”或“H2O”)起吸附催化作用。
③反应的化学方程式为__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】对下列实验中出现的异常现象分析合理的是( )
A. 制取CO2气体时,始终收集不到CO2一一收集CO2的集气瓶没盖严
B. 点燃氢气时,发生爆炸一一点燃前可能没有检验氢气的纯度
C. 细铁丝在氧气中燃烧时,集气瓶底炸裂一一收集的氧气不纯
D. 验证空气中氧气含量时.进入集气瓶中的水大于![]() 一一红磷过量
一一红磷过量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验是研究物质性质的重要手段。请根据下列实验回答问题:
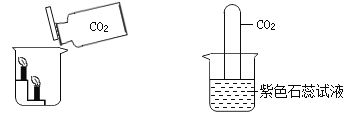
(1)点燃两支梯形架上的蜡烛(如图),沿烧杯内壁缓缓倾倒二氧化碳。实验中,可以观察到的实验现象是_____;该实验说明二氧化碳的物理性质有_____、化学性质有_____。由上述结论可推断 CO2 的重要用途之一是_____。
(2)将一个充满二氧化碳的试管倒插入装有紫色石蕊试液的烧杯里(如图);实验中,可观察到的现象是_____、_____。写出该实验中发生反应的化学方程式_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com