

 3CO2+4H2O,Y的化学式为________,其中各种元素质量比为________.
3CO2+4H2O,Y的化学式为________,其中各种元素质量比为________. 2H2O+O2↑;
2H2O+O2↑; 2Fe+3CO2;
2Fe+3CO2; 3CO2+4H2O,反应后的生成物中含有3个C原子,8个H原子,10个O原子,根据质量守恒定律,反应前也应该含有3个C原子,8个H原子,10个O原子,现在反应前只有10个O原子,故Y中含有3个C原子,8个H原子,故Y的化学式为C3H8,碳、氢元素的质量比为:12×3:1×8=9:2,故填:C3H8,9:2;
3CO2+4H2O,反应后的生成物中含有3个C原子,8个H原子,10个O原子,根据质量守恒定律,反应前也应该含有3个C原子,8个H原子,10个O原子,现在反应前只有10个O原子,故Y中含有3个C原子,8个H原子,故Y的化学式为C3H8,碳、氢元素的质量比为:12×3:1×8=9:2,故填:C3H8,9:2; 2P2O5;
2P2O5;

 53天天练系列答案
53天天练系列答案科目:初中化学 来源: 题型:
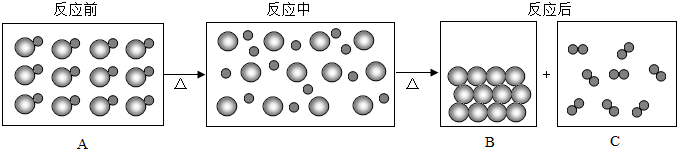
 表示汞原子,
表示汞原子, 表示氧原子,则反应的文字表达式为
表示氧原子,则反应的文字表达式为查看答案和解析>>
科目:初中化学 来源: 题型:
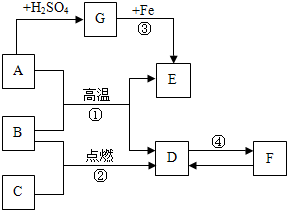 如图A~G是初中化学常见的物质,其中A为黑色固体,E为红色固体单质,B、C、D均为无色气体,F为石灰石的主要成分,G为蓝色溶液,请根据图回答下列问题:
如图A~G是初中化学常见的物质,其中A为黑色固体,E为红色固体单质,B、C、D均为无色气体,F为石灰石的主要成分,G为蓝色溶液,请根据图回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
 如图所示是实验室制取CO2的装置图,根据图回答下列问题.
如图所示是实验室制取CO2的装置图,根据图回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:
 (2012?岳阳一模)图是家用豆浆机,请根据图回答下列问题:
(2012?岳阳一模)图是家用豆浆机,请根据图回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com