
分析 【实验探究一】(1)根据二氧化锰是过氧化氢分解的催化剂,氧气能使带火星的木条复燃分析;
(2)根据二氧化碳能使带澄清石灰水变浑浊,石灰水中的氢氧化钙和二氧化碳反应生成碳酸钙和水,写出反应的化学方程式;
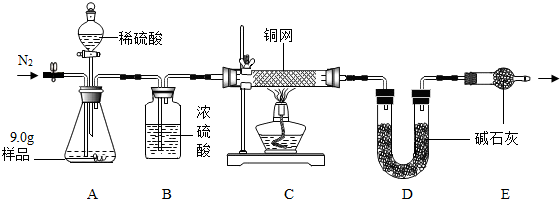
【实验探究二】(3)实验前通氮气是为了除去装置内的空气,以防测定值偏高;实验后还要继续通氮气是为了使残留在装置中的气体全部被吸收;
(4)装置B的作用是干燥气体,防止水分进入D装置使测定值偏大;同时便于观察和控制气流速度以使反应充分进行;
(5)根据E的作用是:防止空气中的二氧化碳进入D装置,否则会使碳酸钠相对含量偏大,影响x:y的比值;
(6)C装置中铜网增重1.2g,则说明生成氧气的质量为1.2g,由氧气质量可计算产品中活性氧含量及过氧化氢质量;D装置增重2.2g说明生成二氧化碳2.2g,计算反应的碳酸钠质量,质量比等于相对分子质量之比计算x与y的比值.
解答 解:【实验探究一】(1)向试管中加入少量MnO2粉末,产生大量气泡.将带火星的木条伸入试管,木条复燃,说明有O2生成,故答案为:O2;
(2)结论有二氧化碳生成,氢氧化钙和二氧化碳反应生成碳酸钙和水,反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O.故答案为:CO2+Ca(OH)2═CaCO3↓+H2O;
【实验探究二】(3)实验前通氮气一段时间,加热铜网至红热后,再缓慢滴入过量稀硫酸,直至A中样品完全反应是为了除去装置内的氧气,以防测定值偏高;实验后还要继续通氮气是为了使残留在装置中的气体全部被装置吸收;故答案为:排出空气,避免产生误差;
(4)装置B的作用是干燥气体,防止水分进入D装置使测定值偏大;同时便于观察和控制气流速度以使反应充分进行;故答案为:ab;
(5)E的作用是:防止空气中的二氧化碳进入D装置,会使碳酸钠相对含量偏大,而不影响过氧化氢的质量,导致x:y的值偏大;故答案为:偏大;
(6)C装置中铜网增重1.2g,则说明生成氧气的质量为1.2g,氧气质量占样品的百分数(活性氧含量)为$\frac{1.2g}{9g}$×100%=13.3%大于13%,属于一等品;
C装置中铜网增重1.2g,则说明生成氧气的质量为1.2g,因为生成氧气的质量为1.2g,则设需要过氧化氢的质量为x
2H2O2~O2↑
68 32
x 1.2g
则$\frac{68}{x}$=$\frac{32}{1.2g}$,解得x=2.55g,故由氧气质量可计算过氧化氢质量为2.55g.
因为D装置增重2.2g,说明生成二氧化碳2.2g,则设需要碳酸钠质量为y
Na2CO3~CO2
106 44
y 2.2g
则$\frac{106}{y}$=$\frac{44}{2.2g}$,解得y=5.3g,故计算反应的碳酸钠质量为5.3g,
根据“产品中活性氧含量测定和过碳酸钠(xNa2CO3•yH2O2)组成”,则可得:106x:34y=5.3g:2.55g,故解得x:y=2:3.
故答案为:13.3;一等品;2:3.
点评 本题属于信息题的考查,主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:初中化学 来源: 题型:选择题
| A. | 对工业污水作处理使之符合排放标准,防止水体污染 | |
| B. | 将废电池填埋,避免重金属污染 | |
| C. | 机动车用压缩天然气替代汽油,减轻空气污染 | |
| D. | 使用微生物降解塑料和光降解塑料,减少白色污染 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滤渣中一定含有铁,一定没有镁、锌 | |
| B. | 得到的滤液一定是无色的 | |
| C. | 滤渣中一定含有铁和锌,一定没有镁 | |
| D. | 滤液中一定含有锌离子和镁离子 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 黄铜(铜锌合金)比铜的硬度小 | |
| B. | 五种金属中,金属铜的导电性最弱 | |
| C. | “金银铜铁锡”是按照金属活泼性由弱到强的顺序排列的 | |
| D. | 五种金属中,只有两种金属能和酸发生置换反应生成氢气 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水是由氢气和氧气两种单质组成 | B. | 水是由氢、氧两种元素组成 | ||
| C. | 水是由氢原子和氧原子组成 | D. | 水分子是由氢元素和氧元素组成 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
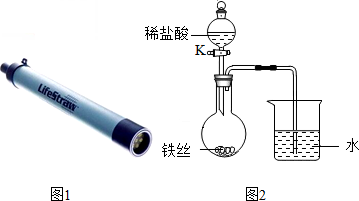 水是最常见的物质之一.
水是最常见的物质之一.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 次序 | 1 | 2 | 3 | 4 |
| 加入稀硫酸的质量/g | 70 | 70 | 70 | 70 |
| 剩余固体的质量/g | 18.2 | 16.4 | x | 13.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com