
 老师用如图所示装置为同学们做如下实验:A装置集气瓶中装有体积比约为1:1的氮气和气体a的混合气体,注射器中装有足量的无色溶液b;B装置中盛有少量紫色石蕊溶液;C装置中盛有适量生锈的铁钉;D装置中盛有足量的稀硫酸.
老师用如图所示装置为同学们做如下实验:A装置集气瓶中装有体积比约为1:1的氮气和气体a的混合气体,注射器中装有足量的无色溶液b;B装置中盛有少量紫色石蕊溶液;C装置中盛有适量生锈的铁钉;D装置中盛有足量的稀硫酸.分析 (1)根据B中溶液进入A中后溶液变为蓝色,说明气体与溶液b反应造成气压降低,且生成了碱性物质进行分析;
(2)由A装置内气压较小,导致B装置内气压也减小,在外界大气压的作用下再分析题目.
解答 解:(1)B中溶液进入A中后溶液变为蓝色,说明气体与溶液b反应造成气压降低,且生成了碱性物质;
①若a气体是二氧化碳,则b必须是能与二氧化碳反应的物质,故可能是氢氧化钠溶液;
②若b是水,则气体a应易溶于水,且溶于水后呈碱性,因此a可能是氨气.
(2)由于A装置中的气体与溶液反应,造成气压减小,B中液体进入A,C中气体进入B,故D中的稀硫酸进入装置C,然后与生锈的铁钉发生反应,反应的化学方程式为:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;Fe+H2SO4=FeSO4+H2↑,由于氢气的生成,气压升高,故长颈漏斗中的液面上升.
故答案为:(1)①NaOH;②NH3;(2)AB;Fe2O3+3H2SO4=Fe2(SO4)3+3H2O、Fe+H2SO4=FeSO4+H2↑.
点评 通过回答本题可知有些题目需要结合物理知识来回答,并且利用外界大气压与瓶内的压力差来做题.


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:初中化学 来源: 题型:实验探究题
| 方案一 | 方案二(数字化实验) |
 | 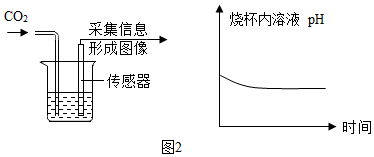 |
| 方案一 | 方案二(数字化实验) |
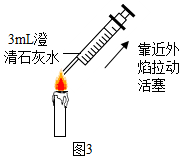 |  |
| 方案一 | 方案二(数字化实验) |
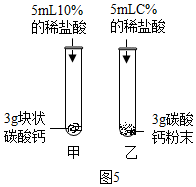 | 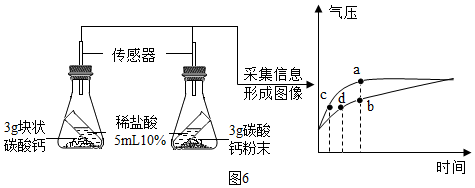 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 为测定某含杂质铜的锌样品中锌的质量分数,取样品20克装入一容器,再取稀硫酸200克,平均分成4份并分4次加入容器中,测定生成气体的总质量,结果如下表:
为测定某含杂质铜的锌样品中锌的质量分数,取样品20克装入一容器,再取稀硫酸200克,平均分成4份并分4次加入容器中,测定生成气体的总质量,结果如下表:| 稀盐酸的质量 | 第一次50g | 第二次50g | 第三次50g | 第四次50g |
| 生成气体总质量 | 0.2g | m | 0.6g | 0.6g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 食盐溶于水,火药爆炸 | B. | 镁带燃烧,铁生锈 | ||
| C. | 食物腐败,水结成冰 | D. | 铁丝被拉长,电灯发光 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 (1)仔细观察图1后回答:该图反映的环境问题是工业的废气不达标排放,形成酸雨使植物死亡;请你提一条合理化建议工业废气达标排放.
(1)仔细观察图1后回答:该图反映的环境问题是工业的废气不达标排放,形成酸雨使植物死亡;请你提一条合理化建议工业废气达标排放.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 凡是有发光、放热现象产生的变化一定是化学变化 | |
| B. | 物质在发生化学变化时,不一定发生物理变化 | |
| C. | 化学变化中一定伴随着放热、发光等现象 | |
| D. | 物质发生物理变化时,不一定发生化学变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com