
【题目】甲、乙、丙三位同学为一家化工厂的污水设计排污方案。请你就他们的探究过程回答有关问题。
Ⅰ.首先用pH试纸检测污水的酸碱性。三位同学分别进行如下实验:
甲:取pH试纸于玻璃片上,用玻璃棒蘸取待测液滴到pH试纸上,测得pH<7。
乙:取pH试纸于玻璃片上,先用蒸馏水润湿,再用玻璃棒蘸取待测液滴到pH试纸上,测得pH<7。
丙:取pH试纸直接浸入待测液中,测得pH<7。
(1)三位同学的操作正确的是________,该污水显________。
Ⅱ.利用中和反应原理测定污水中污染物(盐酸)的质量分数。甲、乙两位同学设计的实验方案图示如下:
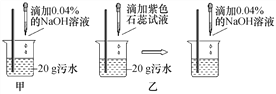
(2)甲同学取少量反应后的溶液于试管中,滴加几滴无色酚酞试液,酚酞试液变红,于是得出“两种物质已恰好中和”的结论。你认为他的结论是否正确?________,理由是_________。
(3)当乙同学观察到_________现象时即恰好完全反应。若此时消耗NaOH溶液2 g,则污水中HCl的质量分数为________。
(4)实验过程中,NaOH溶液必须用胶头滴管逐滴加入,且要用玻璃棒不断搅拌,目的是_________。丙同学利用接在传感器上的计算机绘制出了如下图所示的pH随所加的NaOH溶液体积变化的曲线,从曲线上可知污水的pH=______,M点表示的含义是__________。

(5)除去污水中的盐酸,你建议选用的原料是________。
A.NaOH B.Ca(OH)2 C.CuO D.Fe
【答案】 甲 酸性 不正确 有可能是氢氧化钠溶液过量 溶液由红色变为紫色 0.00365% 防止氢氧化钠过量和使反应充分进行 a 酸碱恰好完全反应(其他合理答案也可) 【答题空10】B
【解析】(1)根据PH值的正确测定方法来考虑,否则测得的结果会产生误差;根据pH和溶液酸碱性的关系分析;(2)根据酚酞试液在碱性溶液为红色分析结论的正确性;(3)根据紫色石蕊试液在酸性、碱性、中性溶液中的颜色分析反应的程度并通过化学方程式进行计算;(4)根据实验的注意事项分析玻璃棒的作用;根据坐标分析;(5)根据酸的性质及可操作性、经济性等分析。(1)测pH值的正确测定方法是:取pH试纸放在玻璃片上,用玻璃棒蘸取待测溶液沾在pH试纸上,将试纸显示的颜色与标准比色卡比较,即可得到pH值,甲操作正确,所以乙同学、丙同学操作都是错误的。用蒸馏水将pH试纸润湿再测该酸性溶液pH值,结果会偏大;将pH试纸直接浸入溶液中会污染试剂;测得废水的pH<7,说明显酸性;(2)根据取少量反应后的溶液于试管中,滴加几滴无色酚酞试液,酚酞变红色,说明此时的溶液显碱性,有可能是氢氧化钠溶液过量;(3)石蕊试液在酸性废水中出现红色,当滴加氢氧化钠的过程中,当溶液由红色变成紫色时恰好完全反应;
设污水中HCl的质量分数为x。
HCl+NaOH═NaCl+H2O
36.5 40
20gx2g×0.04%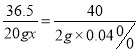
x=0.00365%
所以污水中HCl的质量分数为0.00365%;(4)为了防止氢氧化钠过量,使反应充分进行,实验过程中,NaOH溶液必须用胶头滴管逐滴加入,且要用玻璃棒不断搅拌;从曲线上可知污水的pH=a,即曲线的起点;M点的pH=7,溶液呈现中性,说明酸碱恰好完全反应;(5)A.NaOH;B.Ca(OH)2;C.CuO;D.Fe四种物质都能够和盐酸发生反应,但从经济的角度考虑,氢氧化钙最便宜,故选B。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】如图为KNO3、NaNO2(亚硝酸钠)、NaCl的溶解度曲线,下列说法正确的是
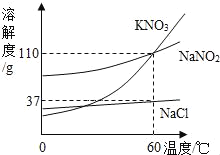
A. KNO3和NaNO2的溶解度相等
B. 60 ℃时,NaCl的饱和溶液的溶质质量分数为37%
C. 将接近饱和的NaNO2溶液变为饱和溶液,可采用降温的方法
D. 除去NaCl中少量KNO3,可在较高温度下制得浓溶液再冷却结晶、过滤、干燥
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图装置是用燃烧法来确定有机物组成的常用装置,这种方法是在电炉加热时用纯氧氧化管内样品,根据产物的质量确定有机物的组成(已知:C中的氧化铜是确保有机物中的碳元素完全转化为二氧化碳;A中的反应为2H2O2![]() 2H2O+O2↑)。
2H2O+O2↑)。
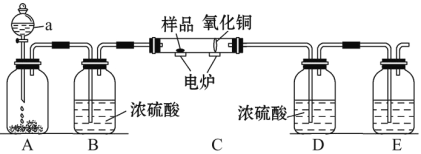
回答下列问题:
(1)a中盛放的物质是 ;
(2)若去掉B装置会对什么元素的测量结果有影响? ,会使测量结果 (填“偏大”或“偏小”);
(3)E装置中所盛放物质最好选用 (选填①氢氧化钙溶液 ②氢氧化钠溶液 ③水);
(4)若准确称取1.12 g样品(样品只含C、H、O三种元素中的两种或三种)。经充分燃烧后,D装置增重1.44 g,E装置增重3.52 g,则该有机物样品中所含的元素为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铝热反应常用于冶炼或焊接金属,其反应原理可表示为3CuO+2Al![]() 3Cu+Al2O3。现将一定量铝粉和氧化铜混合加热,充分反应后停止加热。为了检验氧化铜是否有剩余,取少量反应后的固体,加入足量稀硫酸,反应后将铁片插入上层溶液中。下列叙述的现象,能够说明氧化铜有剩余的是( )
3Cu+Al2O3。现将一定量铝粉和氧化铜混合加热,充分反应后停止加热。为了检验氧化铜是否有剩余,取少量反应后的固体,加入足量稀硫酸,反应后将铁片插入上层溶液中。下列叙述的现象,能够说明氧化铜有剩余的是( )
A. 加热反应结束后有红色物质生成
B. 加入稀硫酸后,有气泡生成
C. 加入稀硫酸后,没有气泡生成
D. 插入溶液中的铁片表面有红色物质生成
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小张同学用某固体物质进行如图所示的实验,根据实验判断下列说法不正确的是( )
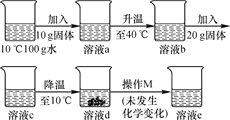
A. 该固体物质的溶解度随温度的升高而增大
B. 溶液b一定是不饱和溶液
C. 溶液d中溶质质量一定大于溶液e中的溶质质量
D. 溶液d和溶液e的溶质质量分数可能相同
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)用化学用语回答:
①氮气分子______;②地壳中含量最多的元素___;③硫酸亚铁中的阳离子是_______;
④二氧化氯(ClO2)是一种常见的漂白剂,标出其中氯元素的化合价___。
(2)下列是实验小组进行的粗盐提纯实验。
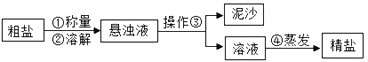
A.操作③的名称是______;操作②③④都用到同一种仪器,它在操作②中的作用是________。
B.工业上通过电解饱和食盐水制备氢氧化钠,化学方程式为:2NaCl + 2H2O ![]() 2NaOH + Cl2↑+ M↑,则M的化学式为__________。
2NaOH + Cl2↑+ M↑,则M的化学式为__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)下列物品所使用的主要材料属于合金的是________(填字母)。
A.青花瓷瓶 B.橡胶充气艇 C.不锈钢锅
(2)生铁是常用的合金,生铁属于________(填“纯净物”或“混合物”)。
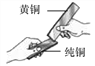
(3)黄铜是铜锌合金,将纯铜片和黄铜互相刻画(如图),纯铜片上留下明显的划痕,说明___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,由此得出的结论错误的是
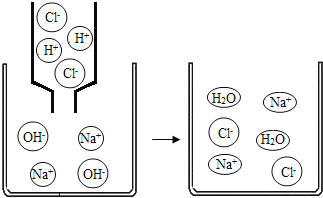
A.反应结束时溶液的pH=7
B.反应前后元素的种类没有变化
C.反应后溶液中存在的粒子只有Na+和Cl﹣
D.该反应的实质是H+和OH﹣结合生成水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】听长辈说制作生拌菜不能添加黄瓜,难道黄瓜能使蔬菜中的营养素流失吗?
【查阅资料】
青椒等蔬菜中含有大量的维生素C,且维生素C能使蓝色的淀粉碘溶液褪色。
【实验操作】
步骤一:淀粉碘溶液的配制:取1克淀粉,加入100毫升水,搅拌均匀,再加入1毫升碘酒溶液;
步骤二:分别榨取新鲜黄瓜汁与青椒汁。各取20毫升青椒汁分别倒入A、B两个锥形瓶中,再分别加入黄瓜汁、蒸馏水各40毫升混匀,放置60分钟,中间每隔10分钟搅拌一次;
步骤三:取等量蓝色淀粉碘溶液分别装入两个烧杯,分别倒入A、B两溶液,搅拌均匀,静置观察。
【现象记录】

根据上述过程回答下列问题:
(1)科学实验需要控制变量,下列情况会影响测定结果的是____。
A.混合液放置时间不同
B.被测混合液的体积不同
C.锥形瓶大小不同
(2)在步骤二中每隔10分钟搅拌一次,其目的是 _________________________。
(3)能证实黄瓜汁把维生素C分解了的实验现象: __________________。
(4)请指出该实验存在的缺陷:_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com