
| A. | R>Cu | B. | R>Fe | C. | Zn>R | D. | R>Ag |
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
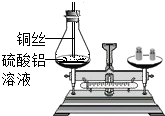 生产实际和实验室有很多金属材料.
生产实际和实验室有很多金属材料.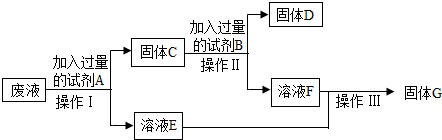
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 化学使人类生活变得更加丰富多彩.
化学使人类生活变得更加丰富多彩.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 使用可降解塑料制品以减少“白色污染” | |
| B. | 霉变的花生清洗后也不能食用 | |
| C. | 香肠中加入较多量的亚硝酸钠防腐 | |
| D. | 废旧报纸、废弃铝制易拉罐放入可回收垃圾箱 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
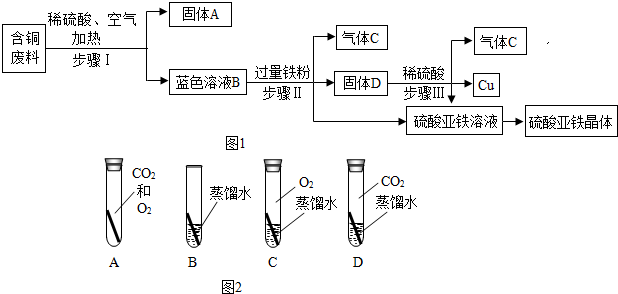
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
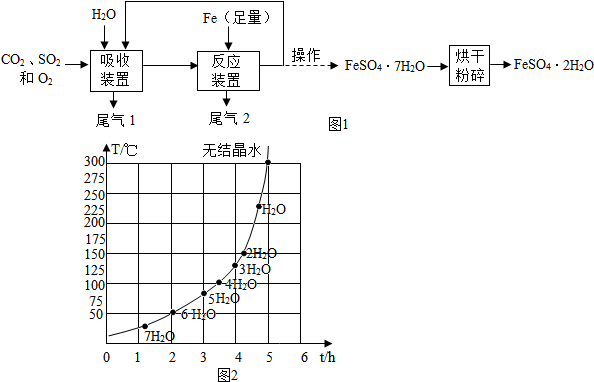
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com