
| A. | 二氧化锰可以使过氧化氢在较低温度下迅速分解产生氧气 | |
| B. | 催化剂只能加快反应速率,而不能减慢反应速率 | |
| C. | 二氧化锰在完全催化后,就失去了催化作用 | |
| D. | 加入二氧化锰可使过氧化氢产生更多氧气 |
分析 在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质叫做催化剂(又叫触媒).催化剂的特点可以概括为“一变二不变”,一变是能够改变化学反应速率,二不变是指质量和化学性质在化学反应前后保持不变.
解答 解:A、二氧化锰可以使过氧化氢在较低温度下迅速分解产生氧气,故选项说法正确.
B、催化剂能改变(包括加快和减慢)化学反应速率,故选项说法错误.
C、二氧化锰在完全催化后,化学性质不变,仍具有催化作用,故选项说法错误.
D、催化剂只能改变化学反应速率,对生成物的质量无影响,使用催化剂不能增加氧气的质量,故选项说法错误.
故选:A.
点评 本题难度不大,考查对催化剂概念的理解,掌握催化剂的特征(“一变二不变”)是正确解答本题的关键.


 高中必刷题系列答案
高中必刷题系列答案科目:初中化学 来源: 题型:选择题
| A. | X一定是排在金属活动顺序表中氢以前的金属 | |
| B. | X是金属时,Y一定是金属 | |
| C. | X是金属时,Y一定比X活泼 | |
| D. | X、Y都是金属时,X一定比Y活泼 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 除杂方法 |
| A | Na2SO4溶液 | NaCl | AgNO3 |
| B | Cu粉 | Fe粉 | 磁铁吸引 |
| C | CaO | CaCO3 | 高温 |
| D | CaCl2溶液 | 稀盐酸 | 加入足量的CaCO3,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 64 | B. | 24 | C. | 40 | D. | 56 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 如图,为测空气中氧气的含量,用一个50ML量筒倒扣在水中,量筒内外液面均位于40ML处.量筒内浮着一个铜制的小船,船中放有少量白磷.现把氢氧化钠缓缓投入水中并搅拌,这样做的原因是NaOH固体溶解于水时放出热量,使溶液温度升高,达到白磷的着火点,放白磷的小船用铜做的原因是铜导热性好且化学性质稳定.一会儿,白磷发生自燃,还可以观察到产生大量白烟,量筒中的液面先下降再上升,最终,液面大约位于量筒刻度32mL处.
如图,为测空气中氧气的含量,用一个50ML量筒倒扣在水中,量筒内外液面均位于40ML处.量筒内浮着一个铜制的小船,船中放有少量白磷.现把氢氧化钠缓缓投入水中并搅拌,这样做的原因是NaOH固体溶解于水时放出热量,使溶液温度升高,达到白磷的着火点,放白磷的小船用铜做的原因是铜导热性好且化学性质稳定.一会儿,白磷发生自燃,还可以观察到产生大量白烟,量筒中的液面先下降再上升,最终,液面大约位于量筒刻度32mL处.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
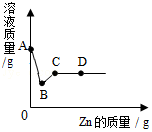 往装有一定质量AgNO3和Cu(NO3)2混合溶液的烧杯中加入Zn,溶液质量与加入Zn的质量关系如图所示.请根据要求回答有关问题.
往装有一定质量AgNO3和Cu(NO3)2混合溶液的烧杯中加入Zn,溶液质量与加入Zn的质量关系如图所示.请根据要求回答有关问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com