
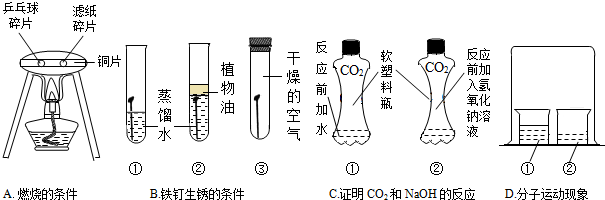
分析 (1)根据燃烧的条件以及铜具有良好的导热性进行解答;
(2)根据铁生锈的主要条件是铁与水和空气直接接触以及除去铁锈可用盐酸清洗方法进行解答;
(3)根据二氧化碳和NaOH溶液反应生成碳酸钠和水进行解答;
(4)根据浓盐酸、浓氨水具有挥发性以及酸碱指示剂遇到酸碱变色情况进行解答.
解答 解:(1)燃烧的条件:物质具有可燃性、与氧气接触、温度达到可燃物的着火点,通过试验A,可以说明燃烧的条件之一是温度达到可燃物的着火点;实验中使用铜片,是利用了铜具有良好的导热性;
(2)对于实验B,一段时间观察试管①中的铁钉明显锈蚀,①试管中即提供了空气,也提供了水,由此得出:铁生锈的主要条件是铁与水和空气直接接触;铁锈的主要成分是氧化铁,所以欲除去铁锈可用盐酸洗方法,铁制品除锈时不能长时间浸在酸溶液中,因为酸也和金属反应;
(3)二氧化碳和NaOH溶液反应生成碳酸钠和水,反应的化学方程式为2NaOH+CO2═Na2CO3+H2O;
(4)实验D的烧杯②中呈现的现象能说明分子是不断运动的.当烧杯①中液体时浓氨水时,浓氨水具有挥发性,挥发出的氨气溶于水显碱性,所以烧杯②中的酚酞溶液由无色变为红色;当烧杯①中液体换成浓盐酸,浓盐酸具有挥发性,挥发出的氯化氢气体溶于水显酸性,烧杯②中液体换成滴有酚酞NaOH溶液时,一段时间后,溶液颜色的变化是红色逐渐褪去变为无色.其中盐酸与NaOH反应生成氯化钠和水,反应的化学方程式为HCl+NaOH═NaCl+H2O,是两种化合物相互交换成分生成另外的两种化合物,属于复分解反应.
故答案为:(1)温度达到可燃物的着火点;导热;(2)空气;盐酸;不能;(3)2NaOH+CO2═Na2CO3+H2O;(4)红;红色逐渐褪去变为无色;HCl+NaOH═NaCl+H2O;复分解.
点评 此题是一道实验设计题,解题的关键是掌握燃烧的条件、铁生锈的条件、二氧化碳的性质、微粒的性质并进行知识的大胆迁移,只有这样才能顺利解题.


科目:初中化学 来源: 题型:解答题
 化学就在我们身边,它与我们的生活息息相关.
化学就在我们身边,它与我们的生活息息相关.查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 盐酸使紫色石蕊溶液变成红色 | B. | 氢氧化钠长期置于空气中变质 | ||
| C. | 酒精用于给发烧病人擦拭降温 | D. | 小苏打在做馒头时用作发酵剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| OH- | CO32- | Cl- | SO42- | NO3- | |
| M2+ | 难溶 | 难溶 | 易溶 | 易溶 | 易溶 |
| A. | M+HCl | B. | MSO4+Ba(NO3)2 | C. | M(OH)2+NaCl | D. | MO+H2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com