
【题目】同学们做了如图四个实验,实验后将4支试管内的物质同时倒入同一烧杯中,发现烧杯中有气泡产生,有白色沉淀。静置,上层溶液为无色。
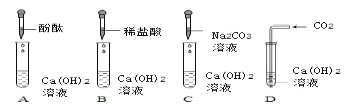
(1)做四个实验的目的是_________________;
(2)以上实验无明显现象的是(填序号)____;
(3)C试管中反应的化学方程式为_________;
(4)下列说法正确的是____________。
A、 最后烧杯中的溶质一定有HCl、NaCl、酚酞
B、 倒入烧杯前,B试管中的溶质是CaCl2和HCl
C、 最终烧杯中的溶液pH=7
D、 为了确定烧杯中溶质的成分,可用碳酸钠溶液
【答案】 探究氢氧化钙的化学性质 B 略 BCD
【解析】(1)由图可知,该实验是多种物质与氢氧化钙反应,故实验目的是探究氢氧化钙的化学性质;
(2)氢氧化钙与稀盐酸反应生成氯化钙和水,该反应中没有明显的现象,故选B。
(3)C试管中是碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应方程式为
Na2CO3+ Ca(OH)2= CaCO3 ↓+2NaOH;
(4)A、4支试管内的物质同时倒入同一烧杯中,发现烧杯中有气泡产生,有白色沉淀,说明稀盐酸和碳酸钙反应,故一定有氯化钙,错误;
B、由题可知,B中稀盐酸有剩余,故B中的溶质有CaCl2和HCl,正确;
C、反应最终有白色沉淀,说明溶液中的稀盐酸反应完全,又因为酚酞不变红,说明溶液的pH小于等于7 ,故最终溶液的pH=7,故正确;
D、碳酸钠与氯化钙反应有白色沉淀生成,故正确。故选BCD;


 智能训练练测考系列答案
智能训练练测考系列答案科目:初中化学 来源: 题型:
【题目】我国化学家侯德榜(如图)改革国外的纯碱生产工艺,生产流程可简要表示如下:


(1)上述生产纯碱的方法称____________________,副产品的一种用途为_________________。
(2)向沉淀池中通入两种气体,先通入的是________________(填“NH3”或“CO2”),沉淀池发生的化学反应方程式是_______________________________。
(3)写出上述流程中X物质的化学式_____________________。
(4)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了_____________(填“循环I”或“循环II”)。从沉淀池中取出NaHCO3沉淀的操作是__________________。
(5)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,先滴加足量的_______,排除Na2CO3的干扰,再滴加___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种固体物质的溶解度曲线如下图所示。回答:
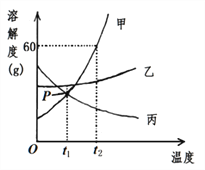
(1)P点表示的意义是:__________;
(2)分别将三种物质的饱和溶液从t2 ℃降至t1 ℃,所得溶液中溶质的质量分数由大到小的顺序是:____;
(3)欲从含少量乙的甲中分离提纯甲,应采用的方法是:______;
(4)t2 ℃时,将50 g甲放入50 g水中,所得溶液的质量是__________g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高氯酸钾( KClO4 ) 可用作火箭推进剂, 其溶解度如下表。下列说法不正确的是
温度 /℃ | 20 | 40 | 60 | 80 |
溶解度 /g | 1.68 | 3.73 | 7.3 | 13.4 |
A.高氯酸钾的溶解度随温度降低而减小
B.20℃时, 将 2g 高氯酸钾溶于 98g 水中, 所得溶液中溶质的质量分数小于 2%
C.60℃时, 高氯酸钾饱和溶液中溶质的质量分数小于 7.3%
D.80℃的高氯酸钾溶液冷却至 40℃肯定有晶体析出
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】分析下图中氯化钠和硝酸钾的溶解度曲线,回答下列问题.
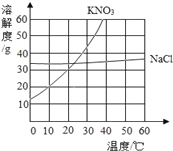
(1)由图可知,硝酸钾的溶解度随温度的升高而______;
(2)20℃时,在100g水中加入40g硝酸钾,充分搅拌后,将溶液温度升高到30℃(不考虑水分蒸发),所得溶液是“饱和”或“不饱和”溶液中的_____________溶液.
(3)若KNO3中混有少量的NaCl,可先将混合物溶于水配成高温下的饱和溶液,然后再采用________(选填“降温结晶”或“蒸发结晶”)的方法就可以提纯KNO3。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】自来水厂净水过程示意图如下,请回答:
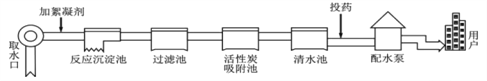
⑴除去水中固态杂质的设备是______(填正确选项前的字母);
A.过滤池 B.吸附池 C.清水池
⑵通常向清水池投放高铁酸钠(化学式为 Na2FeO4)杀菌消毒,高铁酸钠中铁元素的化合价为______;
⑶我国有关部门规定,经上述流程净化后进入用户的饮用水含铁<0.3mg·L-1,含铜<1.0mg·L-1,……。其中的“铁、铜”指的是______(填正确选项前的字母)。
A.原子 B.分子 C.元素
⑷吸附池中利用了活性炭所具有的很强的__________性,该过程属于________变化(填“物理”或“化学”)。
⑸实验室中电解水生成氢气和氧气,说明水是由_________组成的。
⑹生活中可以用_________区别硬水和软水,常采用_________的方法降低水的硬度。
⑺为了清洗餐具上的油污,常在水中加少量洗洁精,洗洁精所起的作用是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学就在我们身边。现有![]() 石墨
石墨![]() 活性炭
活性炭![]() 钛合金
钛合金![]() 碳酸钙
碳酸钙![]() 草木灰
草木灰![]() 二氧化碳,选择适当的物质填空
二氧化碳,选择适当的物质填空![]() 填序号
填序号![]()
![]() 可作气体肥料的是______;
可作气体肥料的是______;
![]() 可用于制造人造骨骼的是______;
可用于制造人造骨骼的是______;
![]() 可作补钙剂的是______;
可作补钙剂的是______;
![]() 可用于去除冰箱异味的是______;
可用于去除冰箱异味的是______;
![]() 可作干电池电极的是______;
可作干电池电极的是______;
![]() 可用作钾肥的是______。
可用作钾肥的是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】从陶瓷、玻璃、水泥到电子芯片,硅元素的用途非常广泛。工业制取高纯硅的部分反应原理的微观示意图如下,有关说法不正确的是
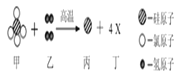
A. 该反应属于置换反应 B. 反应后硅元素的化合价升高
C. 该反应为吸热反应 D. 化学变化中,分子可以再分、原子不可再分
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学习酸碱盐知识后,同学们知道碳酸钠溶液与氢氧化钙溶液能发生反应,可观察到溶液变浑浊。甲组同学进行右图所示的实验,却未观察到预期现象。

【提出问题】未观察到浑浊的原因是什么?
【猜想和假设】
①与氢氧化钙溶液的浓度有关。若使用更大浓度的氢氧化钙溶液,会迅速产生浑浊。
②与碳酸钠溶液的浓度有关。若使用更大浓度的碳酸钠溶液,会迅速产生浑浊。经讨论,同学们认为猜想①不合理,其理由是 。
【进行实验】乙组同学针对猜想②进行实验。
实验目的 | 实验操作 | 实验现象 | |
探究猜想② | 取4支试管,向其中分别加入 | 碳酸钠溶液浓度/% | 是否浑浊 |
10 | 不浑浊 | ||
5 | 不浑浊 | ||
1 | 浑浊 | ||
0.5 | 浑浊 | ||
【解释与结论】
(1)补全上述实验操作:取4支试管,向其中分别加入 。
(2)氢氧化钙溶液与碳酸钠溶液混合出现浑浊的化学方程式是 。
(3)乙组实验证明:猜想②不成立,碳酸钠溶液浓度在0.5~10%的范围内,能否出现浑浊与碳酸钠溶液的浓度有关,其关系是 。
【实验反思】
(1)丙组同学对乙组所做实验中未出现浑浊的原因进行探究。设计了多组实验,其中部分同学的实验过程及结果如下:

丙组同学的实验目的是 。
(2)依据乙、丙两组的实验探究,丁组同学仍使用甲组的仪器和药品对甲组实验进行了改进,当滴入几滴某溶液后,溶液迅速变浑浊。其实验操作是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com