
分析 核裂变和核聚变都能释放能量,对于核裂变是可控的,如核电站的核反应堆就是通过核裂变提供能量的,对于核聚变过程不可控,如氢弹爆炸就是利用核聚变释放能量;从能源是否可再利用的角度可分为可再生能源和不可再生能源.化石能源、核能会越用越少,不可能在短期内从自然界得到补充,所以它们属于不可再生能源.
解答 解:目前核电站是利用核裂变释放的核能来发电的;核能随着使用不断减少,短时间内从自然界得不到补充,因此属于不可再生能源.
故答案为:核裂变;不可.
点评 核能分为裂变和聚变两种,裂变分为两种:可控链式反应和不可控链式反应,前者主要应用在核反应堆中,后者应用在原子弹中;聚变主要应用在氢弹上.


科目:初中化学 来源: 题型:选择题
| A. | 某物质的饱和溶质变为不饱和溶液,溶质的质量分数一定变小 | |
| B. | 任何物质的饱和溶液,当温度降低时,一定会析出溶质 | |
| C. | 在一定温度下,同一物质的饱和溶液一定比不饱和的溶质质量分数大 | |
| D. | 饱和溶液析出晶体后,剩余溶液中溶质的质量分数一定变小 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
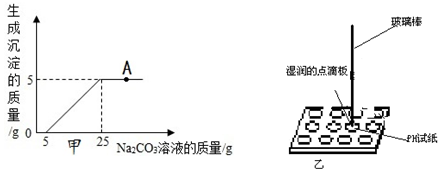
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 一定存在CO32-与NH4+ | B. | 一定不存在Ba2+,可能存在NH4+ | ||
| C. | 一定不存在Na+ | D. | 一定不存在Cl- |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 配制稀硫酸时,用到的玻璃仪器只需量筒和烧杯 | |
| B. | 配制稀硫酸时,一定不能用天平称量所需浓硫酸的质量 | |
| C. | 将480 mL水倾倒入盛有80 mL98%浓硫酸的1000 mL量筒中 | |
| D. | 将80g 98%的浓硫酸沿1000mL烧杯内壁缓缓倒入480 mL水中,并不断搅拌 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 气体 | 吸入空气 | 呼出气体 |
| 氮气 | 78% | 75% |
| X | 21% | 15% |
| 二氧化碳 | 0.03% | 3.68% |
| 水蒸气 | 0.06% | 5.44% |
| 其他 | 0.91% | 0.88% |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
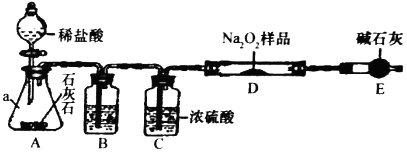
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com