
| 序号 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
| 第1次 | 20 | 11 |
| 第2次 | 20 | 6 |
| 第3次 | 20 | 2.8 |
| 第4次 | 20 | n |
分析 (1)根据图表数据可知,第1、2次反应后固体物质减少的质量都为5g,而第3次反应后固体物质减少的质量为3.2g,说明此时碳酸钙已反应完,不再产生气体,故表中n的数值为2.8.
(2)根据图表数据可知,完全反应后,剩余固体物质的质量为2.8g,石灰石样品的质量减去剩余固体物质的质量就是样品中碳酸钙的质量,然后根据质量分数公式计算即可.
(3)根据碳酸钙与盐酸反应的化学方程式和碳酸钙的质量,即可计算出生成二氧化碳的质量进行解答.
解答 解:(1)根据图表数据可知,第1、2次反应后固体物质减少的质量都为5g,而第3次反应后固体物质减少的质量为3.2g,说明此时碳酸钙已反应完,不再产生气体,故表中n的数值为2.8.
(2)样品中碳酸钙的质量分数=$\frac{16g-2.8g}{16g}$×100%=82.5%.
答:样品中碳酸钙的质量分数为82.5%.
(3)设生成二氧化碳的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
16g-2.8g x
$\frac{100}{16g-2.8g}$=$\frac{44}{x}$
解之得:x=5.8g
答:反应生成的二氧化碳的质量是5.8g.
点评 本题主要考查学生根据反应原理进行分析数据的能力,最后固体质量不减少,即为杂质的质量.


 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁单质 | B. | 铁元素 | ||
| C. | 铁原子 | D. | 铁的相对原子质量 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
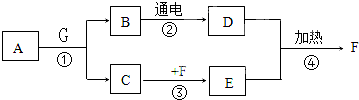
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
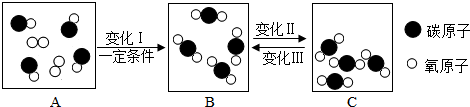
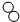 ”和“
”和“ ”的分子个数比为1:2.
”的分子个数比为1:2.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | A将带火星的小木条伸入盛有过氧化氢溶液的试管中 | 有少量气泡 木条不复燃 | 常温下过氧化氢溶液分解速率很慢. |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量Al2O3,然后将带火星的木条伸入试管中 | 产生大量的气泡 木条复燃 | BAl2O3能加快过氧化氢的分解速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com