
| ||
| 100 |
| 44 |
| x |
| 22g |
| 50g |
| 100g×(1-10%) |
| 40 |
| 100 |
| 100g×(1-10%)×40% |
| 78g |


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:初中化学 来源:《8.1 金属矿物与金属冶炼》2010年同步练习(解析版) 题型:解答题
查看答案和解析>>
科目:初中化学 来源:《第5章 金属与矿物》2010年单元测试卷(3)(解析版) 题型:解答题
查看答案和解析>>
科目:初中化学 来源:《第5章 金属与矿物》2010年单元测试卷(2)(解析版) 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:
潍坊市继续实施农村集中供水工程,集中供水覆盖人口已 达到90%以上.自来水厂常用氯气杀毒,用明矾、氯化铁等凝剂净化水.以硫铁矿(主要成分为FeS2)为原料制
达到90%以上.自来水厂常用氯气杀毒,用明矾、氯化铁等凝剂净化水.以硫铁矿(主要成分为FeS2)为原料制 备氯化铁晶体(FeCl3•6H2O)的工艺流程如下:
备氯化铁晶体(FeCl3•6H2O)的工艺流程如下:
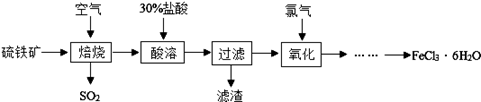
回答下列问题:
⑴流程中需用30%的盐酸“酸溶”焙烧后的残渣(主要成分是氧化铁),写出反应的化学方程式 ,反应的现象是溶液变为 色。
⑵二氧化硫能形成酸雨,危害环境.常用下列方法除去;
方法1.将含二氧化硫的废气通入氨水中吸收二氧化硫.氨水的PH 7(填写“大于”“等于”或“小于”).
方法2.将含有二氧化硫的废气通入石灰石悬浊液中,在空气作用下生成硫酸钙和二氧化碳,从而除去二氧化硫.写出反应的化学方程式: .
⑶自来水厂通常用电解饱和食盐水制备Cl2,反应的化学方程式为:2NaCl+2H2O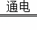 2N
2N aOH+Cl2↑+H2↑.现需要71t氯气用于自来水消毒,理论上需要含杂质10%的粗盐多少吨?同时生成烧碱多少吨?
aOH+Cl2↑+H2↑.现需要71t氯气用于自来水消毒,理论上需要含杂质10%的粗盐多少吨?同时生成烧碱多少吨?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com