
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |


科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
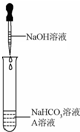 NaOH溶液与NaHCO3溶液混合后无明显现象,同学们产生了疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下实验过程证明NaHCO3溶液与NaOH溶液发生了反应.
NaOH溶液与NaHCO3溶液混合后无明显现象,同学们产生了疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下实验过程证明NaHCO3溶液与NaOH溶液发生了反应.| 实验 | 方法 | NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 |
| 1 | 加入稀盐酸 | 现象Ⅰ | 无明显变化 | 产生气泡 |
| 2 | 加入澄清石灰水 | 溶液变浑浊 | 无明显变化 | 溶液变浑浊 |
| 3 | 加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 | 溶液变浑浊 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 向盛有6g碳酸钠和硫酸钠固体混合物的烧杯中(烧杯质量为20g),加入36.2g稀硫酸,发生反应的方程式为:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑.在一定时间内恰好完全反应,无固体剩余.反应的时间(t)和烧杯及其所盛物质总质量(m)的关系如图所示:
向盛有6g碳酸钠和硫酸钠固体混合物的烧杯中(烧杯质量为20g),加入36.2g稀硫酸,发生反应的方程式为:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑.在一定时间内恰好完全反应,无固体剩余.反应的时间(t)和烧杯及其所盛物质总质量(m)的关系如图所示:查看答案和解析>>
科目:初中化学 来源: 题型:
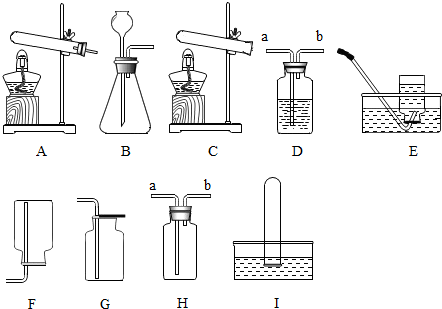
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com