
| A. | 水银一一一Ag | B. | 干冰一一一CO2 | ||
| C. | 小苏打一一一Na2CO3 | D. | 纯碱一一一NaOH |
科目:初中化学 来源: 题型:选择题
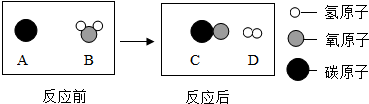
| A. | 生成的两种物质都属于单质 | B. | 生成物的分子个数比为1:1 | ||
| C. | 分子是由原子结合而成的 | D. | 在化学变化中原子不可分 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 打开盛有浓硫酸的试剂瓶塞,瓶口出现白雾 | |
| B. | 浓硫酸不慎沾到皮肤上,立即用大量的水冲洗,然后再涂上3%-5%的碳酸氢钠溶液 | |
| C. | 实验室用稀硫酸和石灰石制取二氧化碳 | |
| D. | 把铜片放入稀硫酸中,产生大量气泡 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
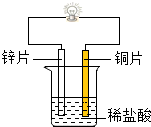 为探究锌、铜、镍三种金属的性质,某兴趣小组进行如下实验,请回答相应问题:
为探究锌、铜、镍三种金属的性质,某兴趣小组进行如下实验,请回答相应问题:| 锌 | 铜 | 镍 | 铜 | |
| 稀盐酸的质量分数 | 3% | 3% | 15% | 15% |
| 反应现象 | 少量气泡 | 无现象 | 许多气泡 | 无现象 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 吸附能使硬水变为软水 | |
| B. | 用纯碱可除去面团发酵产生的酸 | |
| C. | 不能用工业酒精勾兑饮用酒 | |
| D. | 回收废旧金属既节约金属资源,又减少环境污染 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 反应前 | 反应后 | |
| 装置d(含药品)的质量/g | 100.00 | 100.18 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com