
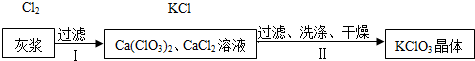
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
分析 (1)根据质量守恒定律以及化学反应中的能量变化来分析;
(2)①根据过滤操作的原理、所需仪器以及注意事项来分析;
②根据图中反应流程,判断找出能与氯化钾反应生成氯酸钾的物质;根据图中所给信息中氯酸钾的溶解度进行分析解答;
③根据饱和溶液是不能再溶解某种溶质的溶液结合反应流程进行分析.
解答 解:(1)反应前有:Ca、2C,反应后有:Ca、2C、4H、2O,所以空格处应为2H2O;乙炔燃烧过程中,化学能转化为了光能与热能;2H2O;发光、放热;
(2)①A.过滤是用来分离难溶性固体与液体的常用方法,故正确;
B.过滤需要普通漏斗而不是长颈漏斗,故错误;
C.过滤操作中,玻璃棒的下端要紧靠在三层滤纸一侧,故错误;
D.过滤器内的液面要低于滤纸的边缘,故正确;
故填:AD;
②由图中反应流程氯化钾加入到氯化钙和氯酸钙混合物中发生反应,根据复分解反应发生的条件,氯化钙与氯化钾不反应,故氯化钾只能与氯酸钙反应生成氯酸钾;由题中物质在常温下的溶解度表中数据发现氯酸钾的溶解度较小,故生成氯酸钾由于常温下氯酸钾溶解度较小,所以过量的氯酸钾会结晶析出;故填:Ca(ClO3)2;
③通过分析可知,Ⅱ中析出晶体后的母液是KClO3的饱和溶液,最后得到的母液中含有KClO3、没有参与反应的CaCl2、生成的KCl以及Ca(ClO3)2.
故填:饱和;KClO3、CaCl2、KCl、Ca(ClO3)2
点评 此题综合考查物质的相互转化和制备,掌握质量守恒定律和正确书写化学方程式的方法是解题的关键.


 发散思维新课堂系列答案
发散思维新课堂系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 结论 |
| ①用试管取少量蒸馏水,滴入1-2滴无色酚酞试液 | 试管内溶液不变色 | 猜想1不成立 |
| ②用试管取少量KCl溶液,滴入1-2滴无色酚酞试液 | 试管内溶液不变色 | 猜想2不成立 |
| ③用试管取少量氢氧化钾溶液,滴入1-2滴无色酚酞试液 | 试管内溶液变红 | 猜想3成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
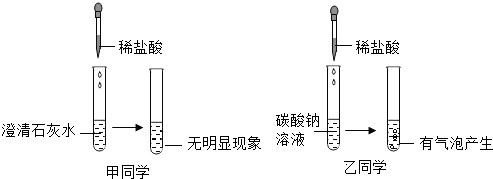
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | YX | B. | Y2X | C. | YX2 | D. | XY |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
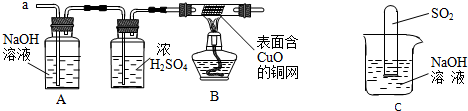
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CO2、CO都不能供给呼吸,都可以充入食品袋防止微生物繁殖从而延长保质期 | |
| B. | 二者的组成元素相同而化学性质不同的原因是原子的排列方式不同 | |
| C. | 当CO2混有少量CO时,可以在适量的氧气中燃烧CO,从而除去CO | |
| D. | CO2可用于制作碳酸饮料、作制冷剂,而CO可用于冶炼金属 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com