
| A. | ①② | B. | ③④ | C. | ②③ | D. | ①④ |
分析 方法一、①根据质量守恒定律,反应前后元素的种类不变,根据计算二氧化碳中的碳元素的质量和根据化学方程式计算,水的质量及其氢元素的质量,确定物质的组成;
②由8.8gCO2,可计算出碳元素的质量,再计算R中碳元素的质量分数;
③根据化学方程式计算,已知6.4g某物质R完全燃烧生成8.8gCO2,可计算生成的水的质量;
④根据化学方程式计算,已知6.4g某物质R完全燃烧生成8.8gCO2,可计算R的相对分子质量.
方法二、由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断反应物R的化学式,进一步分析.
解答 解:方法一、①根据质量守恒定律,反应前后元素的种类不变:8.8g×$\frac{12}{44}$×100%=2.4g;
根据化学方程式计算,设水质量为x,
2R+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+4H2O
88 72
8.8g x
则$\frac{88}{8.8g}=\frac{72}{x}$,x=7.2g,
故氢元素的质量为7.2g×$\frac{2}{18}$×100%=0.8g;
碳元素的质量+氢元素的质量=2.4+0.8<6.4,故R应由碳、氢、氧元素三种元素组成;故①错误;
②由8.8gCO2,可计算出碳元素的质量为:8.8g×$\frac{12}{44}$×100%=2.4g,再计算R中碳元素的质量分数为:$\frac{2.4g}{6.4g}$×100%=37.5%;故②正确
③根据②中计算,故③6.4gR燃烧还生成了7.2gH2O,正确;
④根据化学方程式计算,设R的相对分子质量为y,
2R+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+4H2O
2R 88
6.4g 8.8g
$\frac{2R}{6.4g}=\frac{88}{8.8g}$,
解得R=32.故④R的相对分子质量等于64,错误
故选C.
方法二、根据反应的化学方程式2R+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+4H2O,反应物中氧原子个数分别为6,反应后的生成物中碳、氢、氧原子个数分别为2、8、8,根据反应前后原子种类、数目不变,则2R中含有2个碳原子、8个氢原子和2个氧原子,则每个R分子由1个碳原子、4个氢原子和1个氧原子构成,则物质R的化学式为CH4O.
①R由碳、氢、氧三种元素组成,故错误;
②R中碳元素的质量分数是$\frac{12}{12+4+16}×100%$=37.5%,故正确;
③根据化学方程式计算,设水质量为x,
2CH4O+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+4H2O
88 72
8.8g x
则$\frac{88}{8.8g}=\frac{72}{x}$,x=7.2g,故正确
④R的相对分子质量等于12+(1×4)+16=32,故错误.
故选:C.
点评 要求掌握并理解各元素的相对原子质量的作用;求物质中各元素的比值,计算某分子的相对分子质量,求某物质中某元素的质量分数都是基本的计算.


科目:初中化学 来源: 题型:实验探究题
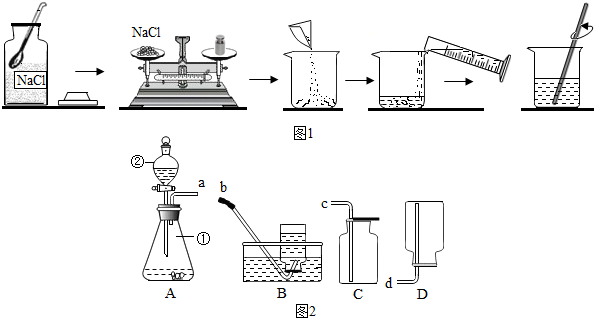
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 在元素周期表中硅元素的某些信息如图所示,下列有关硅的说法错误的是( )
在元素周期表中硅元素的某些信息如图所示,下列有关硅的说法错误的是( )| A. | 属于金属元素 | B. | 元素符号为“Si” | ||
| C. | 原子序数为“14” | D. | 相对原子质量为“28.09” |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 反应前后氢原子、氧原子的个数均不变 | |
| B. | 表示氢气与氧气在点燃的条件下反应生成了水 | |
| C. | 参加反应的氢气与生成的水的分子个数比为1:1 | |
| D. | 参加反应的氢气与参加反应的氧气质量比是2:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
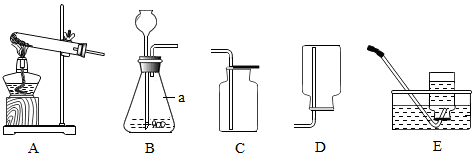
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
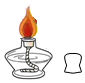 如图是一支燃着的酒精灯(填仪器名称),用它进行加热操作时,应使用火焰的外焰,当开始加热时应检查酒精灯里有无酒精;添加酒精时容积不能超过酒精灯容积的$\frac{2}{3}$,当实验结束需要停止加热时应使用灯帽盖灭.
如图是一支燃着的酒精灯(填仪器名称),用它进行加热操作时,应使用火焰的外焰,当开始加热时应检查酒精灯里有无酒精;添加酒精时容积不能超过酒精灯容积的$\frac{2}{3}$,当实验结束需要停止加热时应使用灯帽盖灭.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com