
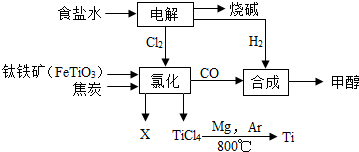
 ij���ÿ���������ұ�������ȼ���״��������һ����ҵ������ͼ��ʾ��������������Դ�����ʣ������˻�����Ⱦ������д��
ij���ÿ���������ұ�������ȼ���״��������һ����ҵ������ͼ��ʾ��������������Դ�����ʣ������˻�����Ⱦ������д�� Сѧ��10���ӿ������100��ϵ�д�
Сѧ��10���ӿ������100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����嫵ĺ�ˮ���̲��ŷḻ�Ļ�ѧ��Դ����ˮ�к���80����Ԫ�� | B��ˮ����Ⱦ��Ӱ�칤ũҵ����ҵ�������ƻ�ˮ��̬ϵͳ | C��Ϊ�˽�Լ��ˮ����ũҵ���ֽ��ࡢ�����Ϊ��ࡢ�ι� | D���ҹ�ˮ��Դ�ḻ���˾�ˮ��������ǰ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
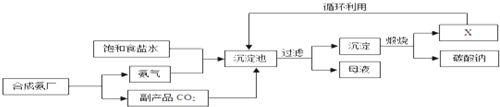
| A���������еķ�Ӧ�ﹲ��������Ԫ�� | B�����˵õ��ġ�ĸҺ����һ��ֻ������������ | C��ͼ��X�����ǰ��� | D��ͨ�백����������ʹ��Һ�ʼ��ԣ��ٽ�������̼�����գ�������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
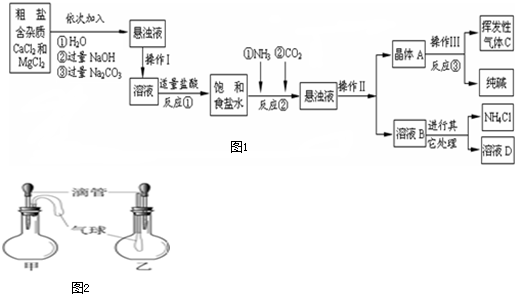
| ||
| ���� | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
| �ܽ�� | 36.0g | 9.6g | 37.2g | 710 | 0.9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ������ | Na2CO3 | NaHCO3 | NaCl |
| ����/kg | 814.8 | 400.3 | 97.3 |
| ������ | Na2CO3 | NaHCO3 | NaCl |
| ����/kg | 137.7 | 428.8 | 97.3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������������������� | B������ϡ���ᷴӦʱ�������û������е����� | C�����ܽ�����ͭ�е�ͭ�û������������������� | D���ڸ���������£������Ѹ�����������������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������̼��̼����ж�����̼Ԫ�أ��������Ƕ����л��� | B������ʳ�ؽ��������ж��ɷ��ü�������ᶾ�� | C��KNO3��KH2PO4�����ڸ��Ϸ� | D�����ۡ���ά�ض��������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com