
| 气体 | 相对分子质量 | 标况下密度(g/L) | 收集方法 |
| 空气 | 29 | 1.293 | 排水集气法 |
| 氧气 | 32 | 1.429 | 向上排空气法 |
| 二氧化碳 | 44 | 1.964 | 向上排空气法 |
| 氢气 | 2 | 0.089 | 向下排空气法 |
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:实验探究题
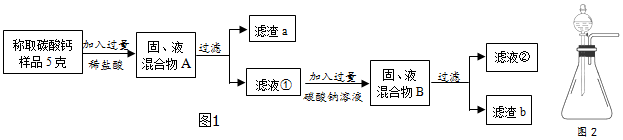
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 28%的稀硫酸中溶质与溶剂的质量比为28:100 | |
| B. | 用lkg 98%的浓硫酸可配制3.5kg 28%的稀硫酸 | |
| C. | 配制该稀硫酸时,把水沿容器内壁缓慢注入浓硫酸中 | |
| D. | 配制好的稀硫酸可以存放在铁制容器中 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 归纳总结是学习的重要方法.小明同学在学习“应用广泛的酸、碱、盐”知识后,结合常见酸(HCl、H2SO4)的性质与变化绘制出如图.图中“-”两端的物质都能够反应,其中酸碱中和反应生成盐和水,则其他连线的产物也都是盐和水的是A-D中的( )
归纳总结是学习的重要方法.小明同学在学习“应用广泛的酸、碱、盐”知识后,结合常见酸(HCl、H2SO4)的性质与变化绘制出如图.图中“-”两端的物质都能够反应,其中酸碱中和反应生成盐和水,则其他连线的产物也都是盐和水的是A-D中的( )| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 食物 | 泡菜 | 葡萄 | 番茄 | 苹果 | 牛奶 | 玉米粥 |
| pH | 3.4 | 4.2 | 4.4 | 3.1 | 6.5 | 7.8 |
| A. | 胃酸过多的人应少食泡菜 | B. | 用湿润的pH试纸蘸取葡萄汁测其pH | ||
| C. | 番茄的酸性比苹果强 | D. | 牛奶和玉米粥均属于碱性食物 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
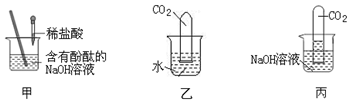
| 实验操作 | 实验现象 | 实验结论 |
| 取少量甲实验所得溶液于试管中,并往试管中加入锌粒 | 观察到有气泡产生 | 猜想2正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
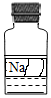 某同学发现了标签部分破损且装有无色溶液的试剂瓶一个(如图),他们想指导内盛的是什么物质,因此,他们进行了如下探究
某同学发现了标签部分破损且装有无色溶液的试剂瓶一个(如图),他们想指导内盛的是什么物质,因此,他们进行了如下探究| 实验方案 | 实验一 | 实验二 | 实验三 |
| 实验操作 |  | 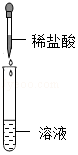 |  |
| 实验现象 | 试纸变色,对照比色卡,pH>7 | 有无色无味气体产生 | 有白色沉淀产生 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
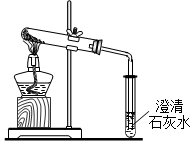 取少量碳酸氢钠(NaHCO3)粉末,用如图装置进行实验,充分加热后发现:大试管中管口有水珠出现,管底有白色固体残留;小试管中澄清石灰水变浑浊.完全反应后,取残留固体溶于水配成溶液,往该溶液中滴加CaCl2溶液,有白色沉淀生成.
取少量碳酸氢钠(NaHCO3)粉末,用如图装置进行实验,充分加热后发现:大试管中管口有水珠出现,管底有白色固体残留;小试管中澄清石灰水变浑浊.完全反应后,取残留固体溶于水配成溶液,往该溶液中滴加CaCl2溶液,有白色沉淀生成.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com