
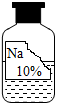
 实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如下图),化学小组的同学经过寻问老师后只知道是NaCl、NaOH、Na2CO3、NaHCO3中的一种溶液,为确认原瓶中是何种溶质并判断其是否变质,化学小组的同学进行了如下的探究活动:
实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如下图),化学小组的同学经过寻问老师后只知道是NaCl、NaOH、Na2CO3、NaHCO3中的一种溶液,为确认原瓶中是何种溶质并判断其是否变质,化学小组的同学进行了如下的探究活动:| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
| 常温下稀溶液的pH | 7 | 13 | 11 | 9 |
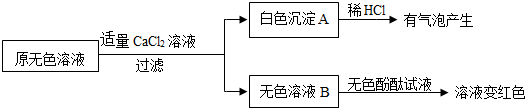
分析 【查阅资料】根据III中所给数据可以求出在20℃时各物质的饱和溶液的质量分数,可以做出判断;
【进行实验】(1)氯化钠溶液呈中性,pH等于7;
(2)根据碳酸钠可以和氯化钙反应生成碳酸钙沉淀和氯化钠解答;可以设计实验来验证碳酸钠的存在;
【获得结论】根据实验现象分析解答.
解答 解:
【查阅资料】根据计算可以知道在20℃时饱和碳酸氢钠的质量分数为:$\frac{9.6g}{100g+9.6g}$×100%=8.8%<10%,所以能够排除碳酸氢钠;故填:碳酸氢钠的饱和溶液溶质质量分数在该温度下不能达到10%;
【进行实验】
(1)测定溶液的pH大于7,而氯化钠溶液呈中性,pH等于7所以不可能是氯化钠,故填:NaCl;
(2)①过量的氯化钙可以检验并除尽碳酸钠,碳酸钠可以和氯化钙反应生成碳酸钙沉淀和氯化钠,产生白色沉淀的化学方程式是Na2CO3+CaCl2=CaCO3↓+2NaCl;故填:Na2CO3+CaCl2=CaCO3↓+2NaCl;
②滴加无色酚酞,滤液变红,说明溶液呈碱性,还有氢氧化钠,实验可以判断原无色溶液中含有的溶质有NaOH、Na2CO3;故填:NaOH、Na2CO3;
【获得结论】该瓶原来装的无色溶液的溶质是NaOH,并且部分变质;故填:NaOH.
点评 本题综合利用了物质的组成、物质的溶解性、溶液的酸碱性及物质的变化规律对未知物质进行鉴别,还考查学生利用化学方程式和溶质质量分数公式进行计算的能力,难度不大,可依据相关物质的性质逐渐分析得出结论.


科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量样品于试管中,加水溶解后再加入少量CaCl2溶液 | 产生白色沉淀 | 假设Ⅱ不成立,反应的化学方程式为Na2CO3+CaCl2═CaCO3↓+2NaCl. |
| 取少量样品于试管中,用导管连接后固定在铁架台上,导管的另一端插入澄清石灰水中.加热样品 | 有气体产生,澄清的石灰水变浑浊 | 假设Ⅰ不成立.则样品的成分是Na2CO3和NaHCO3. |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 温度(℃) | 20 | 40 | 50 | 60 | 80 | |
| 溶解度(g/100g 水) | NaCl | 36.0 | 36.6 | 37.0 | 37.3 | 38.4 |
| NH4Cl | 37.2 | 45.8 | 50.4 | 55.2 | 65.6 | |
| KNO3 | 31.6 | 63.9 | 85.5 | 110 | 169 | |

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 温度/℃ | 10 | 30 | 50 | 70 | 90 |
| 溶解度/g | 27.7 | 39.3 | 49.0 | 54.1 | 51.1 |
| A. | 硫酸镁的溶解度随温度升高而增大 | |
| B. | 10℃时,27.7g硫酸镁和72.3g水可配制成质量分数为27.7%的硫酸镁溶液 | |
| C. | 50℃时,100g的硫酸镁饱和溶液中溶质和溶剂的质量比为49:100 | |
| D. | 70℃时的硫酸镁饱和溶液升温至90℃,溶液的溶质质量分数增大 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
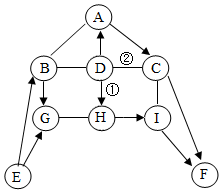 如图中A-I表示初中化学常见的物质,且分别是由一种或两种元素组成:其中A、B、D、H均为单质;F可用作大棚蔬菜生产中的气体肥料;H在B、F、G存在的情况下可以生成铜绿[铜绿主要成分为Cu2(OH)2CO3].图中“--”表示两端的物质间能发生化学反应:“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去.
如图中A-I表示初中化学常见的物质,且分别是由一种或两种元素组成:其中A、B、D、H均为单质;F可用作大棚蔬菜生产中的气体肥料;H在B、F、G存在的情况下可以生成铜绿[铜绿主要成分为Cu2(OH)2CO3].图中“--”表示两端的物质间能发生化学反应:“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 室温下的氯化钠饱和溶液不能再溶解氯化钾 | |
| B. | 取出部分上层溶液,可将接近饱和的氯化钠溶液变为饱和 | |
| C. | 可用硝酸银溶液鉴别氯化钠和氯化镁溶液 | |
| D. | 将100g质量分数为20%的氯化钠溶液稀释为10%,所用的仪器有:烧杯、量筒、玻璃棒和胶头滴管 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com