
分析 (1)根据质量守恒定律,反应前后减少的质量为氧气的质量进行解答.
(2)利用分解过氧化氢制氧气的化学方程式,根据氧气的质量求出过氧化氢的质量,进而求出过氧化氢溶液中溶质的质量分数即可.
解答 解:(1)生成氧气的质量是50.0g+2.0g-50.4g=1.6g;故填:1.6;
(2)设:该过氧化氢溶液中溶质的质量为x
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 1.6g
$\frac{68}{x}=\frac{32}{1.6g}$
x=3.4g
此过氧化氢溶液中,溶质的质量分数为:$\frac{3.4g}{50g}$×100%=6.8%
答:此过氧化氢溶液中溶质的质量分数为6.8%.
点评 本道题目比较简单,是一道最基本的根据化学方程式的计算题,解题关键是根据质量守恒定律求出氧气的质量.


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
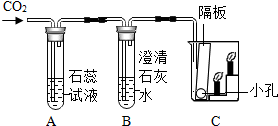 康康同学设计了如图装置验证二氧化碳的性质,当通入二氧化碳一段时间后,A中发生反应的化学方程式为为CO2+H2O=H2CO3;C中观察到蜡烛由低到高依次熄灭,说明二氧化碳的性质有二氧化碳的密度比空气大、不燃烧、不支持燃烧.(答出2条即可).
康康同学设计了如图装置验证二氧化碳的性质,当通入二氧化碳一段时间后,A中发生反应的化学方程式为为CO2+H2O=H2CO3;C中观察到蜡烛由低到高依次熄灭,说明二氧化碳的性质有二氧化碳的密度比空气大、不燃烧、不支持燃烧.(答出2条即可).查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com