
 (2013?闵行区一模)水和溶液在生命活动和生产、生活中起着十分重要的作用.回答下面有关水的问题.
(2013?闵行区一模)水和溶液在生命活动和生产、生活中起着十分重要的作用.回答下面有关水的问题.| 98g |
| 20% |
| 390g |
| 1g/mL |


科目:初中化学 来源: 题型:
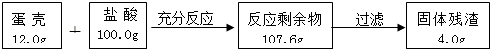
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
| 编号 | KClO3质量/g | 其他物质质量/g | 待测数据 |
| 实验1 | 5.0 | ||
| 实验2 | a | MnO2 1.5 |
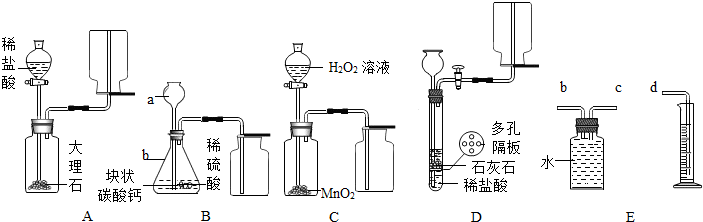
查看答案和解析>>
科目:初中化学 来源: 题型:
| 1 |
| 5 |
| ||
| ||
| ||
| ||
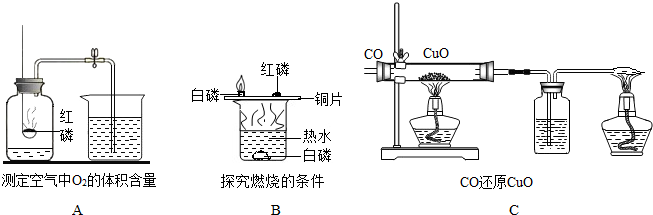
查看答案和解析>>
科目:初中化学 来源: 题型:
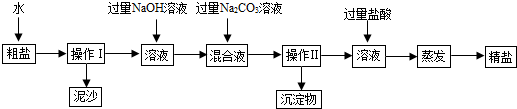
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| ||
| 实验步骤 | 实验现象 | 结论 | |
| 步骤A | 将加热后的固体放入水中,搅拌、静置. | 底部有大量白色不溶物 | 剩余固体中含有碳酸钙 |
| 步骤B | 取上层清液,滴加无色酚酞试液. | 变红 | 剩余固体中含有 CaO CaO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com