
科目:初中化学 来源: 题型:
 32、32、水通常是用来灭火的,但有时却能引火.将少量超氧化钾(KO2)粉末用棉花包裹没有任何变化.(已知棉花和KO2不反应),但将少量水滴到包有KO2粉末的棉花上,则迅速发生剧烈反应,可使瓶内棉花燃烧(比在空气中燃烧还剧烈).
32、32、水通常是用来灭火的,但有时却能引火.将少量超氧化钾(KO2)粉末用棉花包裹没有任何变化.(已知棉花和KO2不反应),但将少量水滴到包有KO2粉末的棉花上,则迅速发生剧烈反应,可使瓶内棉花燃烧(比在空气中燃烧还剧烈).查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| 加热 |
| 加热 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
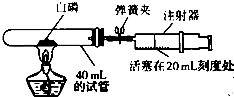 小雅同学通过学习,对空气和氧气有了一定的了解:
小雅同学通过学习,对空气和氧气有了一定的了解:| 第一组 | 第二组 | 第三组 | |||||||||
| 集气瓶编号 | ① | ② | ③ | ④ | ⑤ | ① | ② | ③ | ④ | ⑤ | ① |
| 收集的O2占容积的体积分数(%) | 10 | 20 | 30 | 40 | 50 | 3l | 33 | 35 | 37 | 39 | 34 |
| 带火星木条的 状况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 | 很亮 | 很亮 | 复燃 | 复燃 | 复燃 | 很亮 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| 验证方法 | 现象 | 判断 | |
| 猜想I:主要成分 为氯化铵 |
取少量滤液加入NaOH固体,并加热 | 未闻到明显的氨的刺激性气味 | 猜想I不成立 猜想I不成立 |
| 猜想Ⅱ:主要成分 为氯化锌 |
取少量滤液逐滴滴入稀氨水 取少量滤液逐滴滴入稀氨水 |
先有白色沉淀、后溶解 先有白色沉淀、后溶解 |
猜想Ⅱ成立 |
| 由上述实验得出的结论是:滤液中 主要为氯化锌,其中可能含少量的氯化铵 主要为氯化锌,其中可能含少量的氯化铵 | |||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com