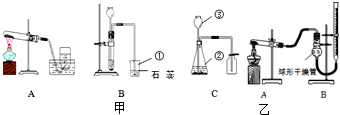
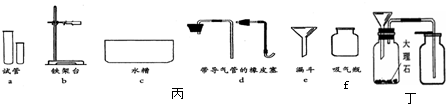
某化学兴趣小组的同学对实验室制取氧气的实验展开了如下探究:

(1)小明同学选用如图1所示的装置制取氧气.制取过程中所发生反应的化学反应方程式为:
.实验前小明同学先向仪器A中加入水,然后将导气管放入水槽中,并打开仪器A的活塞,观察导气管口是否有连续的气泡出现.该实验操作的目的是
检查装置的气密性
检查装置的气密性
.
(2)小雨阅读课外资料得知:双氧水分解除了用二氧化锰还可用氧化铜等物质作催化剂,于是他对氧化铜产生了探究兴趣.
【提出问题】
氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】
小雨以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略).
| 实验序号 |
KClO3质量 |
其他物质质量 |
待测数据 |
| ① |
1.2g |
l |
|
| ② |
1.2g |
CuO 0.5g |
| ③ |
1.2g |
MnO2 0.5g |
①上述实验应测量的“待测数据”是
得到相同质量的氧气所需要的时间
得到相同质量的氧气所需要的时间
.
②若实验②比实验①的“待测数据”更
小
小
(填“大”或“小”),说明氧化铜能加快氯酸钾的分解速率.
③将实验②反应后的固体经提纯分离仍得到0.5克黑色粉末,再将黑色粉末放入试管中,
加入氯酸钾固体加热,一会儿就有气泡冒出
加入氯酸钾固体加热,一会儿就有气泡冒出
(简述操作和现象),说明氧化铜还能作氯酸钾的催化剂.
【评价设计】你认为小雨设计实验③和实验②对比的目的是
比较氧化铜和二氧化锰哪个催化效果更好
比较氧化铜和二氧化锰哪个催化效果更好
.
(3)小林同学对“过氧化氢溶液的浓度对反应速度有何影响”展开如下探究:取不同浓度的过氧化氢溶液,在其他条件相同的情况下进行实验,记录数据如下:
| 实验 |
1 |
2 |
3 |
4 |
5 |
| 过氧化氢溶液的浓度 |
1% |
3% |
5% |
10% |
15% |
| MnO2粉末用量/g |
0.5 |
0.5 |
0.5 |
0.5 |
0.5 |
| 收集到500mL气体时所用时间/秒 |
560 |
186 |
103 |
35 |
12 |
①根据以上数据分析过氧化氢溶液的浓度对反应速度有怎样的影响:
过氧化氢溶液的浓度越大,反应的速度越快
过氧化氢溶液的浓度越大,反应的速度越快
;
②小芳同学验证实验后二氧化锰的质量是否仍为0.5g,她取反应后的溶液进行如下操作:
过滤
过滤
、洗涤、干燥、称量,她用如图2所示的装置进行实验,试指出图中的三处错误
用烧杯直接向漏斗内倒液体
用烧杯直接向漏斗内倒液体
;
液面高于滤纸边缘
液面高于滤纸边缘
;
漏斗的下端在烧杯的中央
漏斗的下端在烧杯的中央
.

 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案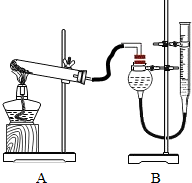 气体为准,其它可能影响实验的因素均已忽略.相关数据见下表:
气体为准,其它可能影响实验的因素均已忽略.相关数据见下表: