
分析 (1)根据红磷和氧气在点燃的条件下生成五氧化二磷,五氧化二磷会污染空气,红磷过量的目的是完全消耗氧气进行分析;
(2)根据铁丝和氧气在点燃的条件下生成四氧化三铁,以及实验过程中的注意事项,铁丝不能在氧气中燃烧进行分析;
(3)根据白磷的着火点低,铜片上的白磷和空气接触,温度达到着火点,会发生燃烧进行分析;
(4)根据浓硫酸稀释的正确操作进行分析.
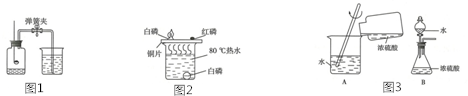
解答 解:(1)红磷和氧气在点燃的条件下生成五氧化二磷,集气瓶中要先加入少量水的作用是:吸收五氧化二磷,防止污染空气,红磷燃烧时可观察到的主要现象是:发出黄色火焰,生成大量白烟,化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,该实验中红磷需稍过量,目的是:充分消耗瓶内的氧气,若实验结束后发现某同学所做实验的广口瓶内水面上升明显小于瓶内空气体积的$\frac{1}{5}$,你认为产生此问题的原因可能是:塞子没有塞紧,冷却不充分;
(2)在做铁丝在氧气中燃烧的实验时,集气瓶中要先加入少量水的目的是防止溅落的熔化物炸裂瓶底,铁丝要盘成螺旋状的目的是增大铁丝的受热面积,集气瓶中的现象是:铁丝在阳气重剧烈燃烧,火星四射,放出大量的热,有黑色固体生成,该反应的化学方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.铁丝不能用于“测定空气中氧气含量”的实验,原因是:铁丝在空气中不能燃烧;
(3)白磷的着火点低,铜片上的白磷和空气接触,温度达到着火点,会发生燃烧,铜片上的红磷没有达到着火点,水中的白磷没有与氧气接触,所以观察到的现象是:铜片上的白磷燃烧,生成大量白烟,而铜片上的红磷和水中的白磷不燃烧,烧杯中热水的作用是:提供热量,并使水中的白磷隔绝氧气;
(4)稀释浓硫酸时,应将浓硫酸加入水中,并用玻璃棒不断搅拌,
①稀释浓硫酸操作正确的是A,
②如图3A中玻璃棒的作用是:搅拌散热,B中玻璃导管的作用是:调节锥形瓶内外气体压强,防止塞子冲开.
故答案为:(1)吸收五氧化二磷,防止污染空气,发出黄色火焰,生成大量白烟,4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,充分消耗瓶内的氧气,塞子没有塞紧,冷却不充分;
(2)防止溅落的熔化物炸裂瓶底,增大铁丝的受热面积,火星四射,黑色固体,3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.不能,铁丝在空气中不能燃烧;
(3)铜片上的白磷燃烧,生成大量白烟,而铜片上的红磷和水中的白磷不燃烧,提供热量,并使水中的白磷隔绝氧气;
(4)①A,
②搅拌散热,调节锥形瓶内外气体压强,防止塞子冲开.
点评 熟练掌握测定空气中氧气含量实验的过程、注意问题、会分析实验现象得出结论是解答本题关健.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:初中化学 来源: 题型:解答题
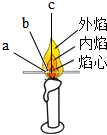 某同学对蜡烛及其燃烧进行了如下的探究:
某同学对蜡烛及其燃烧进行了如下的探究:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
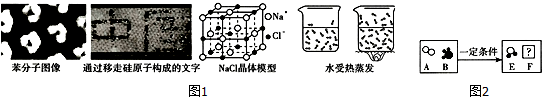
| A | B | C | D | |
| 微观示意图 | 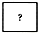 |  |  |  |
| 化学符号 | 2O2 | 3NH3 | ? | / |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
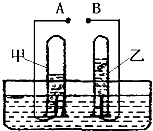 如图是电解水的实验装置图,请根据你所了解的知识填空:
如图是电解水的实验装置图,请根据你所了解的知识填空:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
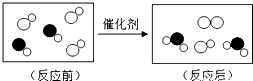 如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法错误的是( )
如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法错误的是( )| A. | 此反应的反应实质是原子重新组合 | |
| B. | 此化学反应有三种新物质生成 | |
| C. | 原子在化学变化中不可再分 | |
| D. | 参加反应的两种分子的个数比为1:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| 物质 | X | Y | Z | M |
| 反应前质量 | 60g | 5g | 10g | 2g |
| 反应后质量 | a | 5g | 32g | 20g |
| A. | a等于20g | B. | Y一定是催化剂 | ||
| C. | X参加反应的质量为20g | D. | 该反应属于分解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com