
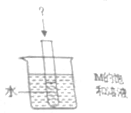
 已知M物质和氯化钠的溶解度与温度的关系如表所示
已知M物质和氯化钠的溶解度与温度的关系如表所示| 温度/℃ | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | 物质M | 32.2 | 37.4 | 40.4 | 50.4 | 55.2 |
| 氯化钠(NaCl) | 35.7 | 35.8 | 36 | 36.3 | 36.6 | |
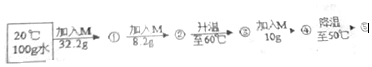
分析 (1)根据图表数据可知氯化钠的溶解度受温度影响情况;
(2)根据20℃时M的溶解度及溶质的质量分数计算式分析解答;
(3)根据饱和溶液中溶质的质量分数=$\frac{溶解度}{100g+溶解度}$×100%,及图表二者的溶解度分析解答.
(4)根据溶液为饱和溶液以及M物质的溶解度随温度的升高而增大进行解答;
(5)根据过滤适用于不溶性固体物质的分离进行解答.
(6)并根据饱和溶液的定义及M在不同温度下的溶解度判断溶液的状态.
解答 解:(1)由图表数据可知氯化钠的溶解度受温度影响小;
(2)溶液①是在20℃时向100水中加入M32.2g,通过图表可知20℃时M的溶解度是32.2g,说明此时形成的溶液恰好是饱和溶液,溶质M的质量分数是$\frac{32.2g}{132.2g}$×100%≈24.4%;
(3)依据上表信息,当温度在20℃~30℃这一范围时,二者的溶解度可能相同,可在同一温度下,配制出溶质质量分数相等的M和NaCl的饱和溶液;
(4)根据题意:烧杯中盛放着30℃的M的饱和溶液,试管中有适量水,向试管中加入一种固体,过一会儿烧杯底部有少量M的晶体析出,说明M的溶解度减小;观察图表可知:M的溶解度随温度的升高而增大,说明在试管中加入的物质溶解吸热,使溶液温度降低,溶解度减小;分析选项,试管中加入冰块、干冰和硝酸铵可使溶液温度降低,氯化钠溶于水溶液温度变化不大,氧化钙和氢氧化钠溶于水使溶液的温度升高,故选ACD;
(5)过滤适用于不溶性固体物质的分离,碳酸钙和铁粉不溶于水,能用溶解、过滤、蒸发的方法分离.
(6)20℃时M的溶解度是32.2g,20℃时向100水中加入M32.2g恰好饱和,所以溶液①②均为饱和溶液;60℃时M的溶解度是55.2g,而加入溶质的质量是32.2g+8.2g=40.4g,所以③是不饱和溶液;再加入10g,溶质为50.4g,故④依然不饱和,50℃时M的溶解度是50.4g,所以降温至50℃时溶液恰好饱和;
故答案为:(1)小;
(2)24.4%;
(3)20~30;
(4)ACD;
(5)AC;
(6)①②⑤;
点评 本题较为综合的考查了学生对溶解度含义的理解应用、根据图表获取信息,并据饱和溶液、不饱和溶液分析解答,及对溶质质量分数的掌握和解决问题的能力.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 泡沫塑料、海绵是可燃物 | |
| B. | 泡沫塑料、海绵的着火点很高 | |
| C. | 燃烧产生的浓烟中含有大量有毒气体 | |
| D. | 着火时应尽快湿布捂住口鼻,撤向安全处 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 厨房内煤气泄漏打开排气扇通风 | B. | 冬天用煤取暖时封闭门窗 | ||
| C. | 在煤窑中挖煤用火把照明 | D. | 油锅中的油着火用锅盖盖灭 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
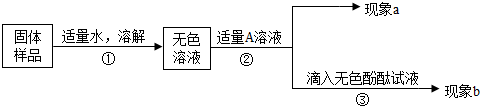
| 实验方案 | A 测溶液pH | B滴加Na2CO3溶液 | C滴加BaCl2溶液 |
| 实验操作 | 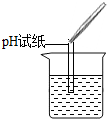 | 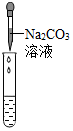 | 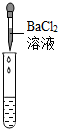 |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 产生有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液显酸性 | 溶液中有H2SO4剩余 | 溶液中有H2SO4剩余 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
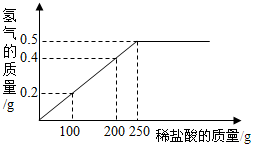 现有铜粉和镁粉的混合物样品,某兴趣小组要测定样品中镁的质量分数.他们称取该混合物样品10g置于烧杯中,然后加入350g一定质量分数的稀盐酸.所加稀盐酸的质量与产生氢气的质量关系如图所示.请计算:
现有铜粉和镁粉的混合物样品,某兴趣小组要测定样品中镁的质量分数.他们称取该混合物样品10g置于烧杯中,然后加入350g一定质量分数的稀盐酸.所加稀盐酸的质量与产生氢气的质量关系如图所示.请计算:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 | |
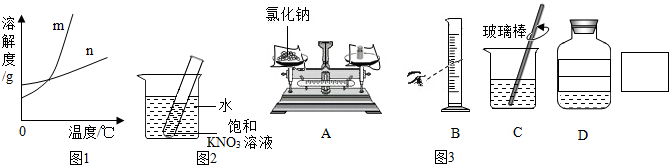
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com