
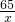 =
=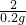


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:初中化学 来源: 题型:阅读理解


| 实验操作 | 实验现象 | 结论 |
| I.取少量的金属粉末于试管中,加入足量的 氢氧化钠溶液 (填试剂名称). |
有气泡产生(或固体减少) |
仅除去铝 |
| II.将试管静置,弃去上层清液,加入足量的稀硫酸. | 有气泡产生(或固体减少或产生浅绿色溶液). |
证明含有铁 |
| III.将试管静置,弃去上层清液,加水,多次洗涤剩余固体 | 剩余固体呈紫红色 | 证明含有铜 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 金属是现代生活和工业生产中应用极为普遍的一类材料.
金属是现代生活和工业生产中应用极为普遍的一类材料.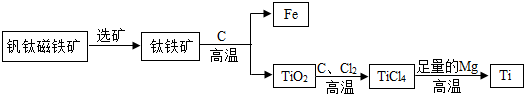
| 实验操作 | 实验现象 | 结论 |
| Ⅰ取少量的金属粉末于试管中,加入足量的 |
仅除去铝 | |
| Ⅱ将试管静置,弃去上层清液,加入足量的稀硫酸. | 证明含有铁 | |
| Ⅲ将试管静置,弃去上层清液,多次洗涤剩余固体 | 剩余固体呈紫红色 | 证明含有铜 |
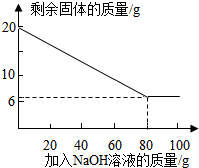 ②为探究该金属粉末中Al的质量分数,取20 g该金属粉末,把100 g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据与图象如下:
②为探究该金属粉末中Al的质量分数,取20 g该金属粉末,把100 g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据与图象如下:| 加NaOH溶液的次数 | 第一次 | 第二次 | 第三次 | … |
| 剩余固体的质量/g | 16.5 | n | 9.5 | … |
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
 2010年7月3日,紫金矿业位于福建上杭县的紫金山铜矿湿法厂发生污水渗漏事故,9100立方米废水外渗引发福建汀江流域污染,造成沿江上杭、永定出现鱼类死亡和水 质污染现象.某校化学兴趣小组的同学对河水取样,欲探究其酸碱性并想出处理措施.
2010年7月3日,紫金矿业位于福建上杭县的紫金山铜矿湿法厂发生污水渗漏事故,9100立方米废水外渗引发福建汀江流域污染,造成沿江上杭、永定出现鱼类死亡和水 质污染现象.某校化学兴趣小组的同学对河水取样,欲探究其酸碱性并想出处理措施.| 所需药品或试剂 | 步骤或方法 | 可能观察到的现象 | 得出结论 |
紫色石蕊试液 紫色石蕊试液 |
将河水静置,取上层清液于试管中,滴加紫色石蕊试液,振荡,观察现象 将河水静置,取上层清液于试管中,滴加紫色石蕊试液,振荡,观察现象 |
紫色石蕊试液变红 紫色石蕊试液变红 |
河水呈酸性 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验步骤 | 实验现象 | 结论 |
| 取少量反应后的溶液于试管中, 加入碳酸钠溶液 加入碳酸钠溶液 . |
有气泡产生 |
稀盐酸过量. |
| 实验步骤 | 实验现象 | 结论 |
| 取少量反应后的溶液于试管中, 加入稀盐酸 加入稀盐酸 . |
有气泡冒出 有气泡冒出 |
恭喜你!你的猜想正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com