


科目:初中化学 来源: 题型:阅读理解

| 猜想 | 简单实验方案 | 现象 | CO和CuO反应的化学方程式 |
| 粉末为Cu | 不反应 | CuO+CO=Cu+CO2 | |
| 粉末溶解,溶液变成蓝色,生成红色粉末 | 2CuO+CO=Cu2O+CO2 |

查看答案和解析>>
科目:初中化学 来源: 题型:
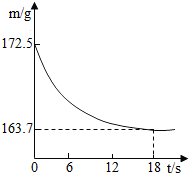 某公司生产出的纯碱产品中经检测只含有氯化钠杂质.为测定产品中碳酸钠的质量分数,20℃时,称取该产品样品26.5g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液.反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如下图所示.
某公司生产出的纯碱产品中经检测只含有氯化钠杂质.为测定产品中碳酸钠的质量分数,20℃时,称取该产品样品26.5g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液.反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如下图所示.查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 紫色石蕊试液 | pH<5.0:红色 | 5.0<pH<8.0:紫色 | pH>8.0:蓝色 |
| 无色酚酞试液 | pH<8.2:无色 | 8.2<pH<10.0:红色 | pH>10.0:无色 |
| 温度/°C | 10 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 64 | 85 | 138 | 203 | 285 | 376 |
| 106 |
| x |
| 73 |
| y?7.3% |
| 44 |
| 2.2g |
| 13.5g-5.3g |
| 13.5g |
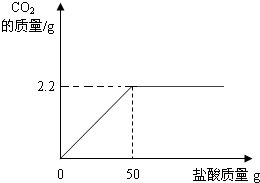
| 106 |
| x |
| 73 |
| y?7.3% |
| 44 |
| 2.2g |
| 13.5g-5.3g |
| 13.5g |

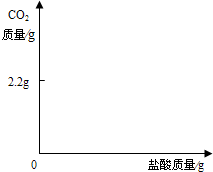
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
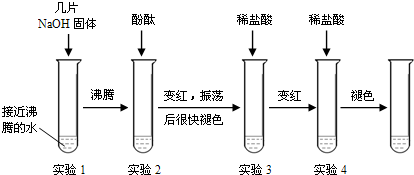
| 实验操作 | 实验现象 | 实验结论 | |
| 猜想 | 在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水,充分振荡 | 固体粉末全部溶解 固体粉末全部溶解 |
猜想a、c不成立,猜想b成立. |

| 实验操作 | 主要实验现象 | 实验结论及解释 | |
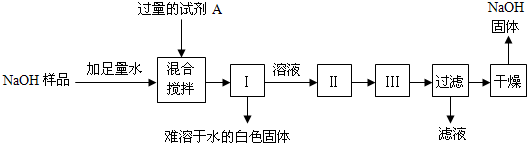
| ① | 检查装置的气密性. 向装置中加入药品. |
装置的气密性良好. | |
| ② | 打开分液漏斗活塞,向A 装置中缓慢加入稀盐酸. |
A装置中观察到的现象有 有大量的气泡产生 有大量的气泡产生 ,C装置中有气泡出现. |
A装置中发生反应的化学方程式为 CaCO3+2HCl=CaCl2+H2O+CO2↑ CaCO3+2HCl=CaCl2+H2O+CO2↑ ;C装置作用是 除去没有反应的二氧化碳 除去没有反应的二氧化碳 . |
| ③ | 一段时间后用带火星的木条在D内进行检验. | 带火星的木条复燃. | 过氧化钠与二氧化碳反应并生成氧气. |

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
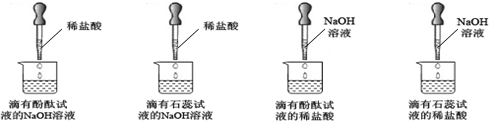
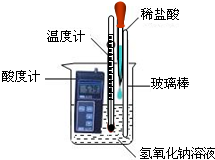 化学调研小组的同学用氢氧化钠和稀盐酸探究中和反应,请你参与以下探究:
化学调研小组的同学用氢氧化钠和稀盐酸探究中和反应,请你参与以下探究:| 实验方法 | 可能看到的现象 | 结论 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com