为改善城市环境,提升生活质量,建设生态宝应,我县陆续使用天然气,乙醇汽油等清洁能源.
(1)镇江市区家用燃料的更新历程如下:

①下列有关家用燃料更新的理由,正确的是
.
A.天然气是可再生的能源
B.气体燃料的利用率更高
C.减少煤燃烧过程中产生的污染物
②天然气(主要成分是甲烷)和液化石油气(主要成分是丙烷和丁烷)中碳元素的质量分数分别约为75%和82.3%,通过该数据分析:相同条件下,用天然气作燃料比液化石油气更环保的理由
.
③甲烷在空气中完全燃烧的化学方程式为
.
(2)从新疆输送到镇江气门站的天然气需经过除杂、添加无毒臭味剂、减压等处理后才能输送到市民家中.用分子的观点解释天然气减压后体积会膨胀的原因
.在其中添加无毒臭味剂可以起到的作用是
.
(3)为进一步提升空气质量,我县将逐步推广乙醇汽油的使用.所谓乙醇汽油是在汽油中加入适量乙醇混合而成的一种燃料.
①乙醇汽油属于
(选填:“纯净物”或“混合物”).
②从环境保护的角度看,下列燃料中最理想的是
(填写字母编号).
A.氢气 B.煤 C.乙醇汽油 D.煤气(主要含CO)
(4)为测定原煤中的含碳量需要用纯氧气.但小亮同学在实验室制氧气的过程中发现:收集的氧气占集气瓶容积的60%(空气占40%)时,能使带火星的木条复燃.那么,使带火星的木条复燃的氧气浓度的最低值是多少呢?小亮对此展开探究:
第一组实验:取5只集气瓶,编号为①、②、③、④、⑤,分别装入其总容积10%、20%、30%、40%、50%的水.用排水法收集氧气,恰好把5只集气瓶中的水排去.将带火星的木条依次插入①~⑤号瓶中,记录实验现象.
小亮在前一组实验的基础上又做了第二组和第三组实验,三组实验的数据和现象见下表.
| 组别 |
一 |
二 |
三 |
| 集气瓶编号 |
① |
② |
③ |
④ |
⑤ |
① |
② |
③ |
④ |
⑤ |
① |
| 瓶中O2占容积的体积分数(%) |
l0 |
20 |
30 |
40 |
50 |
3l |
33 |
35 |
37 |
39 |
34 |
| 带火星木条的状况 |
微亮 |
亮 |
很亮 |
复燃 |
复燃 |
很亮 |
很亮 |
复燃 |
复燃 |
复燃 |
很亮 |
请根据实验回答下列问题:
①使用带火星的木条验满氧气的方法是否可靠:
(填“是”或“否’').
②收集的氧气占容积的体积分数最低为
%时,可使带火星的木条复燃,这时集气瓶中氧气的体积分数分数是
%(计算结果保留整数).
③采取“半值法”探究能减少实验次数.例如:第一组实验若按③、④的编号顺序进行实验,即可确定下一组实验收集的氧气占容积的体积分数应在30%~40%之间,从而省去编号为①、②、⑤的实验.同理,第二组实验可以省去的实验编号为
.
(5)鉴于用收集好氧气再进行实验,存在上述不确定因素,因此小亮和同学们决定采用下列装置进行测定(如图1):
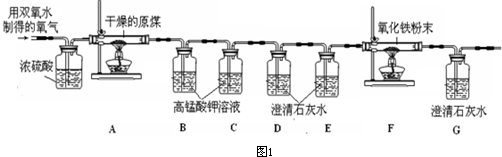
资料:①干燥原煤燃烧产生的气体主要是CO
2,但同时含有少量SO
2和CO;
②SO
2能与高锰酸钾(KMnO
4)反应而使溶液紫红色褪去,也能使澄清石灰水变混浊;而CO
2和CO均不能使紫红色高锰酸钾溶液褪色.请根据装置图2回答:
①浓硫酸的作用是
(选填A或B). A、干燥气体 B、除去气体中碱性物质
②试写出B装置和C装置的作用:B装置的作用
;C装置的作用
.
③若将B、C装置中改成澄清石灰水,D、E装置中改成高锰酸钾溶液,测得原煤中碳元素的质量分数
(填“偏大”或“偏小”).
④F中反应的化学方程式
.
⑤尾气应如何处理?
.
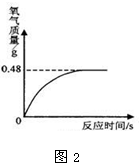
(6)过氧化氢溶液长期保存会自然分解,使得溶质质量分数减小.为确保实验时双氧水的用量.小亮和同学们事先对实验室提供的过氧化氢溶液进行了溶质质量分数测定.他们取出该溶液51g,加入适量二氧化锰,生成氧气的质量与反应时间的关系如图2所示.
①完全反应后生成氧气的质量为
g.
②计算该过氧化氢溶液中溶质的质量分数.



 阅读快车系列答案
阅读快车系列答案

