
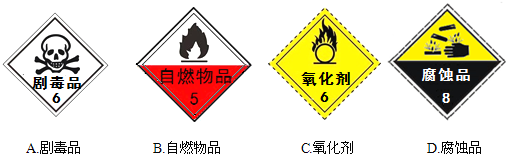
分析 (1)从过氧化氢的化学性质进行分析.
(2)①根据反应物的状态和反应条件确定发生装置;
②从是否节约药品、操作是否简便、是否方便使用等角度考虑;
③根据催化剂的概念分析.
④根据化学方程式的书写方法分析.
⑤根据氧气验满的方法进行解答;
(3)根据质量守恒定律:在化学反应中,反应前后原子的种类没有改变,数目没有增减,进行解答.
解答 解:(1)从过氧化氢的化学性质分析:具有强氧化性.贮运过氧化氢的试剂箱上最适合粘贴的一张标识是 C;
故答案为:C;
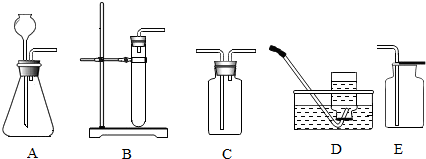
(2)①根据反应物的状态是固态和液态,反应条件是常温,应选固-液的发生装置为A或B;
②加入药品通常采用“把过氧化氢溶液缓缓加入盛有少量MnO2的反应容器中”,优点是:能获得平稳的氧气流(或便于控制产生气体的速率,控制反应进程,或防止反应过快);
③根二氧化锰是过氧化氢制氧气的催化剂,催化剂在化学反应前后质量和化学性质都不变,所以MnO2可以连续反应使用;
④根据书写化学方程式的步骤:写配注等,化学反应方程式为:2H 2O 2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O 2↑;
⑤根据氧气验满的方法:带火星的木条靠近瓶口,木条复燃,即收集满了;
故答案为:A或B; 能获得平稳的氧气流(或便于控制产生气体的速率,控制反应进程,或防止反应过快);
MnO2是催化剂; 2H 2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O 2↑; 带火星的木条靠近瓶口,木条复燃,即收集满了;
(3)根据质量守恒定律:在化学反应中,反应前后原子的种类没有改变,数目没有增减,依据反应的化学方程式为
X+8H2O2=2CO2↑+N2↑+12H2O,推测X的化学式为:C2N2H8;
故答案为:C2N2H8 .
点评 该题从实验室制取氧气的实践出发,考查许多可能出现的问题,对于学生掌握制取氧气的方法以及实践活动都有积极的指导意义.


 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:初中化学 来源: 题型:解答题
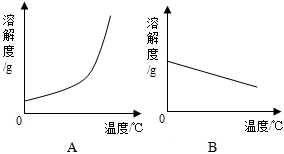
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
| 3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 从空气中获取纯净的氮气,用硫燃烧除去空气中的氧气 | |
| B. | 鉴别硬水和软水,观察颜色或闻气味 | |
| C. | 除去混在二氧化碳中的氯化氢气体,把混合气体通过足量的氢氧化钠溶液 | |
| D. | 鉴别硝酸铵和氯化钠固体加适量的水溶解,测量前后温度变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 金属材料与人类的生产和生活密切相关.请回答:
金属材料与人类的生产和生活密切相关.请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com