
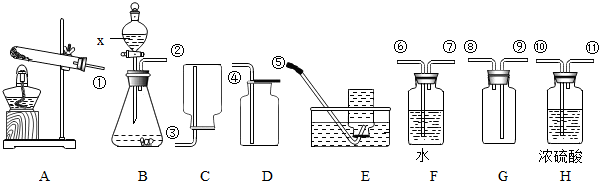
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳可以用浓硫酸干燥;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集.
解答 解:(1)如果用氯酸钾制氧气就需要加热,故答案为:A;
(2)实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集;若用G装置收集氢气,则②应与短管相连,因为氢气的密度比空气的密度小,故答案为:稀硫酸;⑧;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳可以用浓硫酸干燥;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;故答案为:B;H;D;
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了气体的干燥等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.


科目:初中化学 来源: 题型:选择题
| 金属 | 铜 | 锌 | 锡 | 铅 | 铋 | 镉 |
| 熔点/℃ | 1083 | 419.6 | 231.9 | 327.5 | 271.3 | 320.9 |
| A. | 20~40℃ | B. | 60~80℃ | C. | 230~250℃ | D. | 300~320℃ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 葡萄糖是一种有甜味、易溶于水的白色粉末状固体,化学式是C6H12O6.葡萄糖在人体内被缓慢氧化为二氧化碳和水,并释放出热量.试回答:
葡萄糖是一种有甜味、易溶于水的白色粉末状固体,化学式是C6H12O6.葡萄糖在人体内被缓慢氧化为二氧化碳和水,并释放出热量.试回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CaOCl2 | B. | (NH3)2Fe(SO4)2 | C. | Mg(OH)Cl | D. | K3Fe(CN)6 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 结论 |
| 用试管取该溶液1-2mL,滴入1-2滴无色酚酞试液,振荡 | 无色酚酞试液变红. | 溶液呈碱性 |
| 无色酚酞试液不变色 | 溶液呈中性或酸性. |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 在自然界里大多数金属是以化合物的形式存在的.常用的金属冶炼是通过氢气、一氧化碳、碳粉与金属氧化物在高温下反应来实现的.请回答以下有关问题:
在自然界里大多数金属是以化合物的形式存在的.常用的金属冶炼是通过氢气、一氧化碳、碳粉与金属氧化物在高温下反应来实现的.请回答以下有关问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NH4Cl | B. | NaNO3 | C. | K2CO3 | D. | NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
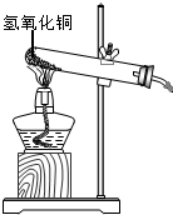 氢氧化铜固体受热分解能得到两种产物,其中一种为固体,某兴趣小组为确定这种固体产物,进行了如下探究活动.
氢氧化铜固体受热分解能得到两种产物,其中一种为固体,某兴趣小组为确定这种固体产物,进行了如下探究活动.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com