
| A. | 完全反应得到无色溶液,样品中一定没有铁 | |
| B. | 反应后过滤,一定会有滤渣 | |
| C. | 所加稀盐酸中溶质的质量分数为7.3% | |
| D. | 反应后过滤,得到溶液中溶质只有氯化镁 |
分析 假设这13g全部为锌,根据化学方程式计算出生成氢气为0.4g,所以剩余的金属中必须假设都是13g时产生氢气的质量必须有比0.4g大的,有比0.4g小的.再进行进一步分析即可.
解答 解:A、因为得到无色溶液,所以一定没有铁,故正确.
B、若样品全部为锌产生氢气质量为0.4g,由于样品中含有杂质,也产生了0.4g氢气,所以样品中一定含有相同质量时比锌产生氢气多的金属,即一定含有镁,且锌、镁的质量和小于13g,所以样品还含有不与盐酸反应的铜.反应后过滤一定有滤渣,故正确.
C、假设这13g全部为锌,设生成氢气质量为x,稀盐酸中溶质的质量分数y,则:
Zn+2HCl═ZnCl2+H2↑
65 73 2
13g y x
则$\frac{65}{13g}=\frac{2}{x}$=$\frac{73}{100gy}$,解得x=0.4g,y=14.6%
根据氢气质量计算出的氯化氢质量为14.6g,所以盐酸的溶质质量分数为14.6%,故错误.
D、滤液中含有氯化镁和氯化锌.根据金属活动性顺序可知:镁>锌>铁>铜,盐酸先和镁反应,在和锌反应,故错误.
故选AB.
点评 解答本题的关键是运用假设法,假设5.6g全部是一种金属,看生成氢气的质量的多少,再进行进一步分析.


 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案科目:初中化学 来源: 题型:解答题
 在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行研究.
在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行研究.| 方案 | 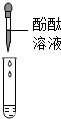 |  |
| 现象 | 溶液变红 | 产生 |
| 结论 | 清液中有氢氧化钠 | 清液中有碳酸钙 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
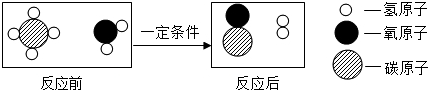
| A. | 反应前后各元素的化合价均不变 | B. | 反应物是混合物,生成物是纯净物 | ||
| C. | 该反应生成物的分子个数比为1:1 | D. | 该反应中含氢元素的化合物有2种 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
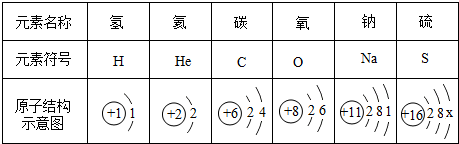
| 反应前 | 反应后 |  | ||
| A | B | C | D | |
 | 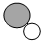 |  | ? | |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
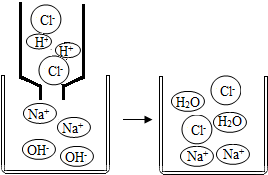 中和反应是一类重要的反应.根据要求回答问题:
中和反应是一类重要的反应.根据要求回答问题:| 操作 | 现象 | 结论 |
| 实验1:往装有碳酸氢钠溶液的试管中先加入2-3滴酚酞溶液,再逐滴加入盐酸直至恰好完全反应 | 滴入酚酞时的现象:酚酞变成红色; 逐滴加入盐酸的现象:有气泡冒出,且溶液逐渐变成无色. | 两者反应时,碳酸氢钠溶液碱性消失 |
| 实验2:往装有盐酸的试管中先加入2-3滴酚酞溶液,再逐滴加入足量的碳酸氢钠溶液 | 酚酞不变色;加入碳酸氢钠,溶液中出现气泡,无色酚酞变成红色. | 两者反应时,盐酸溶液酸性消失 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
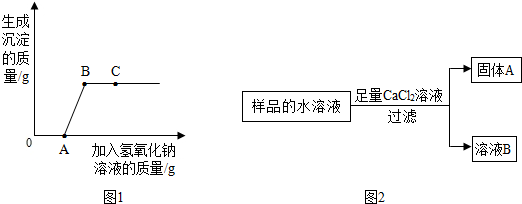
| 实验步骤 | 可能观察到的现象 | 结论 |
| ①取样于试管中,加水溶解,滴入过量的 BaCl2 (填化学式)溶液 | 产生白色沉淀 | 猜想二正确 |
| ②反应后过滤,取上层清液,滴入酚酞溶液 | 溶液不变色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com