
| 物质 | 杂质 | 除杂质所用试剂和方法 | |
| A | CO2 | HCl | 先通入氢氧化钠溶液,后通过浓硫酸 |
| B | Na2CO3溶液 | Na2SO4 | 加入适量的Ba(NO3)2溶液,过滤 |
| C | K2SO4 | Na2CO3 | 加入适量的稀硫酸,蒸发结晶 |
| D | FeCl2溶液 | CuCl2 | 加入过量的铁粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、CO2和HCl气体均能与NaOH溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
B、Na2CO3溶液和Na2SO4均能与适量的Ba(NO3)2溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、Na2CO3能与适量的稀硫酸应生成硫酸钠、水和二氧化碳,能除去杂质但引入了新的杂质硫酸钠,不符合除杂原则,故选项所采取的方法错误.
D、过量的铁粉能与CuCl2溶液反应生成氯化亚铁溶液和铜,再过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选:D.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:初中化学 来源: 题型:多选题
| 物质 | 杂质 | 除去杂质所用的试剂和方法 | |
| A | Na2CO3溶液 | NaOH | 通入适量二氧化碳 |
| B | Cu(OH)2固体 | CuCl2 | 加入适量稀盐酸 |
| C | HNO3溶液 | HCl | 加适量的AgNO3溶液,过滤 |
| D | CO气体 | CO2 | 通过灼热的氧化铜 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
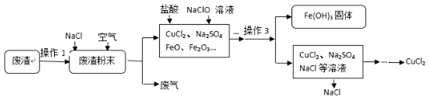
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 试管:我被摔碎了 | |
| B. | 铁钉:我在潮湿空气中最容易生锈啦 | |
| C. | 灯泡:我通电后发光了 | |
| D. | 蜡烛:我受热融化,遇冷又凝固了 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 近年,我国科学家首次拍摄到水分子团簇图象,也成为聚合水(H2O)n,n的数值通常在8~10之间,通过一定的手段将泉水的小分子团水活化,形成3--6个分子或单分子的微分子团,分子团越小渗透力、溶解力、扩散力越强,其分子模型如图.下列说法正确的是( )
近年,我国科学家首次拍摄到水分子团簇图象,也成为聚合水(H2O)n,n的数值通常在8~10之间,通过一定的手段将泉水的小分子团水活化,形成3--6个分子或单分子的微分子团,分子团越小渗透力、溶解力、扩散力越强,其分子模型如图.下列说法正确的是( )| A. | 用微分子团配置的溶液不均一、不稳定 | |
| B. | 团簇中的水分子不再运动 | |
| C. | 用微分子团洗衣服不仅浪费水,还洗不干净衣服 | |
| D. | 若将某温度下用普通水配置的硝酸钾饱和溶液中的溶剂 换成等质量的微分子团水将变成不饱和溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 盐酸和碱之间发生的反应不一定是中和反应 | |
| B. | 工业冶炼铝和生产生石灰的反应类型相同 | |
| C. | NH4NO3中氮元素的化合价相同 | |
| D. | CO${\;}_{3}^{2-}$离子也能使酚酞试液变红色 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
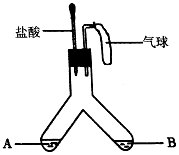 甲、乙、丙三种化学常见物质,由氢、碳、氧、钠、钙、铁6钟元素中的1-4种组成.
甲、乙、丙三种化学常见物质,由氢、碳、氧、钠、钙、铁6钟元素中的1-4种组成.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com