
| A. | 酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 | |
| B. | 碱的水溶液显碱性,所以碱性溶液一定是碱溶液 | |
| C. | 氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物 | |
| D. | 碳酸钠、碳酸钙能与稀盐酸反应,所以所有的碳酸盐都可以与稀盐酸反应 |
分析 A、根据中和反应是酸与碱作用生成盐和水的反应解答;
B、根据碱的水溶液通常呈碱性,但是碱性溶液不一定是碱的溶液进行解答;
C、根据氧化物是指含有两种元素,其中一种是氧元素的化合物进行解答;
D、根据碳酸盐不论是否溶于水,都能与盐酸反应生成二氧化碳解答.
解答 解:
A、酸碱中和反应能生成盐和水,生成盐和水的反应不一定是中和反应,如CO2+2NaOH═Na2CO3+H2O,故错误;
B、碱的水溶液通常呈碱性,但是碱性溶液不一定是碱的溶液,有的盐溶液也呈碱性,例如碳酸钠溶液呈碱性,故错误;
C、氧化物是指含有两种元素,其中一种是氧元素的化合物,所以含氧元素的化合物不一定是氧化物,例如氯酸钾含有氧元素,但不是氧化物,故错误;
D、碳酸盐不论是否溶于水,都能与盐酸反应生成二氧化碳 故正确.
答案:D
点评 本题考查了常见概念的推理,完成此题,可以依据概念进行,所以要求同学们在平时的学习中加强概念的识记及理解,以便灵活应用.


科目:初中化学 来源: 题型:选择题
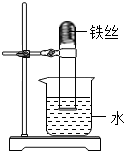 某校化学兴趣小组的同学按照如图装置进行实验,小组同学对实验现象的记录正确的是( )
某校化学兴趣小组的同学按照如图装置进行实验,小组同学对实验现象的记录正确的是( )| A. | 铁丝表面有红色氧化铁附着 | B. | 铁丝光亮,没有变化 | ||
| C. | 试管中的液面无变化 | D. | 试管内液面上升 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 测得pH分别为5.3、7.8 | |
| B. | 将被测液滴到湿润的pH试纸上测定 | |
| C. | 测得pH分别为5、8 | |
| D. | 测得一种溶液的pH=0,由此可知它为中性溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铝合金灯柱属于合成材料 | |
| B. | 硅电池板中的硅元素属于非金属元素 | |
| C. | 灯泡中填充氮气作保护气 | |
| D. | 透明的塑料灯罩属于有机合成高分子材料 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 物质是由元素组成的 | |
| B. | 物质的组成结构变了,也就变成了新物质 | |
| C. | 所有的物质的都是由分子构成的 | |
| D. | 原子也能构成物质 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 实验操作 | 实验现象 | 结论 |
| 用试管取该溶液1-2mL,滴入1-2滴无色酚酞试液,振荡 | 无色酚酞试液变红 | 溶液呈碱性 |
| 无色酚酞试液不变色 | 溶液呈中性或酸性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com