
 字词句段篇系列答案
字词句段篇系列答案科目:初中化学 来源: 题型:解答题
 某补钙剂说明书的部分信息如图所示.小明对该补钙剂十分感兴趣,取10片钙片放入100g稀盐酸中,有效成分刚好完全反应(其他成分不与盐酸反应),剩余物质总质量
某补钙剂说明书的部分信息如图所示.小明对该补钙剂十分感兴趣,取10片钙片放入100g稀盐酸中,有效成分刚好完全反应(其他成分不与盐酸反应),剩余物质总质量查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 ”表示一个氯原子,则“
”表示一个氯原子,则“ ”表示Cl2(填化学符号)
”表示Cl2(填化学符号)查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验方案 | a.测溶液pH | b.滴加Na2CO3溶液 | c.滴加BaC12溶液 |
| 实验操作 | 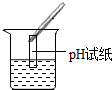 | 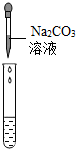 | 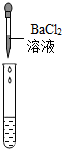 |
| 实验现象 | 试纸变色,对比标准比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 实验课上,为检验镁条能否在N2中燃烧,某兴趣小组开展如下探究:
实验课上,为检验镁条能否在N2中燃烧,某兴趣小组开展如下探究:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com