
【题目】某盐矿井采出的食盐(俗称井盐)中含有CaCl2,为测定CaCl2的含量;准确称量上述井盐22.8g,向其中加入87.2克水使其完全溶解,然后向其中加入10.6%的Na2CO3溶液,生成沉淀的质量与加入Na2CO3溶液的质量关系如图所示(恰好完全反应时所得食盐溶液仍为不饱和溶液)。
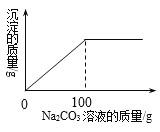
求:⑴井盐中CaCl2的质量分数;
⑵恰好完全反应后所得溶液中NaCl的质量分数(结果都保留一位小数)。
【答案】(1)48.7%;(2)11.7%
【解析】⑴解∶设井盐中CaCl2的质量为xg,反应生成氯化钠质量为yg,生成沉淀zg
Na2CO3 + CaCl2 =CaCO3↓+2NaCl
106 71 100 117
10.6%×100g x z y
![]() =
=![]() ,x=7.1g. 井盐中CaCl2的质量分数∶
,x=7.1g. 井盐中CaCl2的质量分数∶![]() ×100%=48.7%;
×100%=48.7%;
![]() =
=![]() ,y=11.7g.
,y=11.7g. ![]() =
=![]() ,z=10g.
,z=10g.
⑵恰好完全反应后所得溶液中NaCl的质量分数∶![]() ×100%=11.7%.
×100%=11.7%.
答∶⑴井盐中CaCl2的质量分数是48.7%;
⑵恰好完全反应后所得溶液中NaCl的质量分数是11.7%.
点睛∶本题主要考查质量守恒定律的应用以及根据化学方程式进行计算。


 字词句段篇系列答案
字词句段篇系列答案科目:初中化学 来源: 题型:
【题目】我国约在南北朝时就开始冶炼黄铜,黄铜是铜和锌的合金(Cu-Zn),它可用来制造电器零件及日用品。小华利用一瓶稀盐酸和相关的仪器,测定黄铜样品的组成(不考虑黄铜中的其他杂质)。将30mL稀盐酸分三次加入到10g黄铜样品粉末中,每次充分反应后,测定生成氢气的质量,实验数据见下表:
第一次 | 第二次 | 第三次 | |
连续加入盐酸的体积/mL | 10 | 10 | 10 |
生成氢气的质量/g | 0.08 | X | 0.04 |
(1)X=____________;
(2)从上表数据分析,小华用10 g合金粉末总共收集到氢气_______g;
(3)求该合金中铜的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学反应前后,下列各项中,肯定没有变化的是:①原子数目;②原子的种类;③分
子数目;④分子的种类;⑤元素的种类;⑥物质的总质量;⑦物质的种类
A.①②⑤⑥ B.①②③⑤ C.①②⑤⑦ D.③④⑥⑦
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】溶液在生产,生活中应用广泛。下列有关溶液的说法正确的是
A.均一、稳定的液体都是溶液 B.溶液中不能同时存在两种溶质
C.只有固体和液体可以作为溶质 D.外界条件不改变,溶质溶剂不会分离
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示:
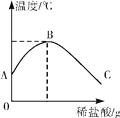
①由图知,稀盐酸与氢氧化钠溶液发生的反应是__________(填“放热”或“吸热”)反应。
②从A到B过程中,烧杯中溶液的pH逐渐_____________。B点表示的含义是___________________。
③在C点处的溶液中加入__________,出现____________________现象,则说明该溶液显________性。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列叙述与对应的坐标图表示正确的是( )
A.  向硝酸钾的饱和溶液中加入氯化钠
向硝酸钾的饱和溶液中加入氯化钠
B. 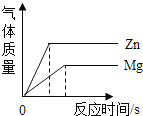 将相同质量的Zn粉和Mg粉分别加入足量的稀盐酸中
将相同质量的Zn粉和Mg粉分别加入足量的稀盐酸中
C. 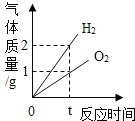 水的电解
水的电解
D.  盐酸和氯化铁混合溶液中加入过量的氢氧化钠溶液
盐酸和氯化铁混合溶液中加入过量的氢氧化钠溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】兴趣小组同学发现实验室一片久置的铜片表面附着有一层绿色固体,查阅资料得知绿色固体是铜绿 [化学式为Cu2(OH)2CO3],能与稀硫酸反应产生硫酸铜、水和二氧化碳,加热产生氧化铜、水和二氧化碳。下面是小组同学回收铜的实验流程:
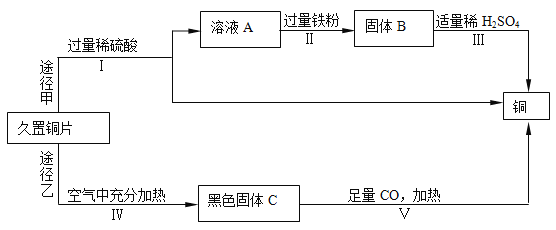
回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ都需要进行过滤的操作,过滤用到的玻璃仪器是烧杯、玻璃棒和 。溶液A所含的溶质有 (填化学式)
(2)写出下列反应的化学方程式:步骤Ⅲ ,步骤Ⅴ 。
(3)同一久置铜片分别通过途径甲和途径乙最终得到的铜的质量是:途径甲 (选填“大于”、“等于”或“小于”)途径乙。
(4)途径甲比途径乙更好的理由是 (答一点)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com