
| ||
| ||


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:初中化学 来源: 题型:
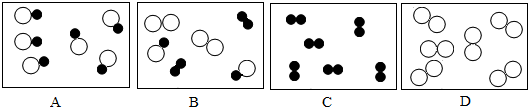
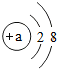 当a=8时,该粒子是
当a=8时,该粒子是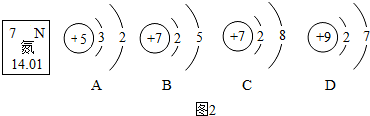
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、单宁酸分子由碳、氢、氧三种元素组成 |
| B、一个单宁酸分子由76个碳原子、52个氢原子和个46个氧原子构成 |
| C、单宁酸中碳、氢、氧三种元素的质量比为38:26:23 |
| D、一个单宁酸分子中含26个氢分子 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
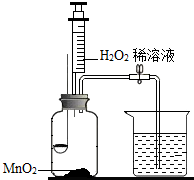 用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验.已知:白磷的着火点为40℃.
用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验.已知:白磷的着火点为40℃.| 内容 步骤 | 【实验1】研究燃烧条件 | 【实验2】研究氧气性质 |
Ⅰ | 烧杯中盛有80℃的热水, 分别在燃烧匙和烧杯中导管口放置一小块白磷,塞紧瓶塞 | 烧杯中盛有NaOH溶液, 燃烧匙中放入木炭点燃木炭后,迅速将燃烧匙伸入瓶中,塞紧瓶塞 |
| Ⅱ | 推入适量H2O2溶液 | 推入适量H2O2溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 今年3月22日是第二十二届“世界水日”,3月22-28日是第二十七届“中国水周”.联合国确定2014年“世界水日”的宣传主题是“水与能源”(Water and Energy).水与人类的生活和生产密切相关.如图为我国《生活饮用水国家标准》的部分内容,请回答下列问题.
今年3月22日是第二十二届“世界水日”,3月22-28日是第二十七届“中国水周”.联合国确定2014年“世界水日”的宣传主题是“水与能源”(Water and Energy).水与人类的生活和生产密切相关.如图为我国《生活饮用水国家标准》的部分内容,请回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com