
 如图为小明学习原子内部结构后制作的某原子结构模型,外圈上的小球代表电子,内圈为原子核.则下列说法中不正确的是( )
如图为小明学习原子内部结构后制作的某原子结构模型,外圈上的小球代表电子,内圈为原子核.则下列说法中不正确的是( )| A. | 该原子的相对原子质量为4 | |
| B. | 该原子的核电核数为4 | |
| C. | 该原子的质量主要集中在原子核上 | |
| D. | 该原子的原子核由2个带正电的质子和2个不带电的中子构成 |
 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:初中化学 来源: 题型:选择题
| 选项 | 物 质 | 杂质 | 试 剂 | 操作方法 |
| A | Cu | CuO | 稀盐酸 | 向混合物中加足量的稀盐酸,充分反应后,过滤,将滤渣洗涤,干燥 |
| B | CO2 | HCl | 氢氧化钠溶液和浓硫酸 | 依次通过盛有足量的两种试剂的洗气瓶 |
| C | MnO2 | KC1O3 | 无 | 把混合物放在试管中加热,使之充分反应 |
| D | Fe | CuSO4 | 蒸馏水 | 加入足量的蒸馏水充分溶解后,过滤,将滤渣洗涤,干燥 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
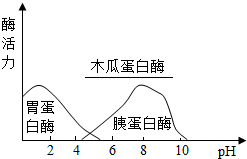 食品种类多,酸碱度范围广,pH对不同蛋白酶的活力影响有差异.作为食品添加剂应该有广泛的酸碱适应范围,木瓜蛋白酶更适宜作为食品添加剂,理由是木瓜蛋白酶的活性不随pH值的变化而变化.
食品种类多,酸碱度范围广,pH对不同蛋白酶的活力影响有差异.作为食品添加剂应该有广泛的酸碱适应范围,木瓜蛋白酶更适宜作为食品添加剂,理由是木瓜蛋白酶的活性不随pH值的变化而变化.| 酶溶液的pH | 1 | 2 | 3 | 4 | 5 |
| 蛋白块消失的时间(min) | 9 | 4 | 7 | 38 | >60 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁 | B. | 氧化铝 | C. | 氧化铁 | D. | 铝 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
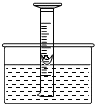 某化学兴趣小组,设计了如图所示装置来研究空气中氮气的体积分数,用一个50mL量筒倒扣在水中,使量筒内内外液面均位于40mL处.量筒内浮着一个铜制的小船,船中放有足量白磷.现把浓硫酸缓缓倒入水中并搅拌.一会儿,白磷发生自燃,量筒内液面上升,向水槽内加水直至量筒内外液面相平,读出此时液面所对刻度.
某化学兴趣小组,设计了如图所示装置来研究空气中氮气的体积分数,用一个50mL量筒倒扣在水中,使量筒内内外液面均位于40mL处.量筒内浮着一个铜制的小船,船中放有足量白磷.现把浓硫酸缓缓倒入水中并搅拌.一会儿,白磷发生自燃,量筒内液面上升,向水槽内加水直至量筒内外液面相平,读出此时液面所对刻度.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
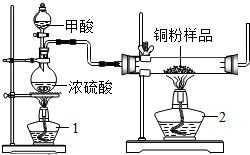 浓硫酸具有脱水性.可以使甲醛(分子式为HCOOH)脱水而获得CO,现拟用如图所示装置(尾气处理部分略)来制取CO,并用CO还原CuO,化学方程式为CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,基于此反应测定某铜粉样品(混有CuO粉末)中金属铜的含量.
浓硫酸具有脱水性.可以使甲醛(分子式为HCOOH)脱水而获得CO,现拟用如图所示装置(尾气处理部分略)来制取CO,并用CO还原CuO,化学方程式为CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,基于此反应测定某铜粉样品(混有CuO粉末)中金属铜的含量.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com